
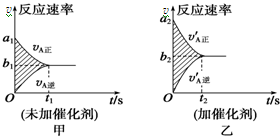
 ���淴ӦmA��g��+nB��g��?pC��g��+gD��g����v-tͼ����ͼ����ʾ�����������������䣬ֻ���ڷ�Ӧǰ������ʵĴ���������v-tͼ����ͼ����ʾ��
���淴ӦmA��g��+nB��g��?pC��g��+gD��g����v-tͼ����ͼ����ʾ�����������������䣬ֻ���ڷ�Ӧǰ������ʵĴ���������v-tͼ����ͼ����ʾ��| A�� | �ڢܢޢ� | B�� | �ڢܢݢ� | C�� | �ڢۢݢ� | D�� | �ڢۢޢ� |
���� ����ֻ�ı䷴Ӧ���ʣ���С�ﵽƽ���ʱ�䣬��ת���ʲ��䣬�Դ������
��� �⣺����ֻ�ı䷴Ӧ���ʣ���С�ﵽƽ���ʱ�䣬��ת���ʲ��䣬
��ͼʹ�ô�������Ӧ���ʼӿ죬���a1��a2����b1��b2��
ʱ�����̣����Ԣ�t1��t2��
��Ӱ���Ϊ��Ӧ��Ũ�ȵı仯�����ڴ�����Ӱ��ƽ���ƶ�������ͼ����Ӱ���������ȣ��ʢ���ȷ��
����ȷ��Ϊ�ڢܢޢߣ�
��ѡA��
���� ���⿼������Է�Ӧ���ʵ�Ӱ�켰ͼ�������Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��ȷͼ����a��b��ʾ��Ӧ���ʵı仯��tΪʱ�伴�ɽ����Ŀ�ѶȲ���


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������0.1 mol•L-1��������Һ�У���NH4Al��SO4��2����NH4Cl����CH3COONH4��c��NH4+�� �ɴ�С��˳��Ϊ�ڣ��٣��� | |
| B�� | ������0.4 mol•L-1CH3COOH��Һ��0.2 mol•L-1 NaOH��Һ�������Ϻ���Һ�����ԣ�����Һ������Ũ���ɴ�С��˳��Ϊc��CH3COO-����c��Na+����c��CH3COOH����c��H+����c��OH-�� | |
| C�� | 0.1 mol•L-1 Na2CO3��Һ��0.2 mol•L-1 NaHCO3��Һ��������������Һ�У�c��CO32-��+2c��OH-��=c��HCO3-��+3c��H2CO3��+2c��H+�� | |
| D�� | 0.1 mol•L-1�İ�ˮ��0.05 mol•L-1 H2C2O4��Һ��������������Һ�У�c��NH4+��+c��NH3•H2O��=2c��C2O42-��+2c��HC2O4-��+2c��H2C2O4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ | B�� | �⻯����Һ | C�� | �Ȼ�������Һ | D�� | ����������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
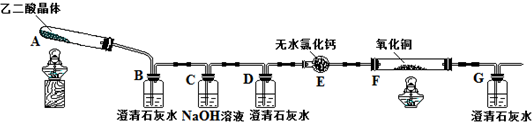
| �ζ�ǰ | ��һ���յ� | �ڶ����յ� | �������յ� | |
| �ζ��� Һ��̶� | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�м���NaHCO3��Һ������ˮ�ĵ��� | |
| B�� | 35��ʱ��ˮ��c��H+����c��OH-�� | |
| C�� | ��ˮ�м���NaHSO4��Һ������ˮ�ĵ��� | |
| D�� | c��H+�������¶ȵ����߶����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
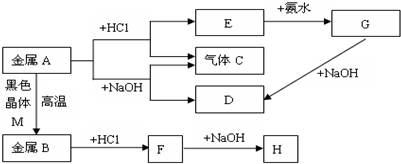
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������¶ȣ����������ݻ��̶����䣬�������ڲ���B���壬����a��b | |
| B�� | �������¶ȡ�ѹǿ���䣬����������壬����a��b | |
| C�� | �������������䣬�����¶ȣ�����a��b | |
| D�� | ��a=b����������ڸ��¶��£����������ݻ��̶���������³����˶������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
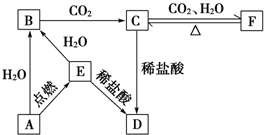
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com