
����Ŀ��ij�¶�ʱ��ˮ�����ӻ����� Kw = 1��10-13�������¶��� pH = 11 �� Ba(OH)2��Һ a L �� pH =1�� H2SO4 ��Һ b L ���(������Һ���Ϊ����֮��������������Բ���)������˵������ȷ����
A. �� a��b = 9��2����������Һ pH ���� 2
B. �� a��b = 9��2���û����Һ������ܽ����� 0.28(a + b) g
C. �����û����ҺΪ���ԣ��� a��b = 1��1
D. �����û����ҺΪ���ԣ����ɳ��������ʵ���Ϊ 0.05b mol
���𰸡�C
��������
A.��a:b=9:2����Ba(OH)2��Һ���Ϊ9L��H2SO4��Һ���Ϊ2L��pH=11��Ba(OH)2��Һ��![]() ����n(OH-)=10-2mol/L��9L=0.09mol��pH =1��H2SO4��Һ��c(H+)=0.1mol/L����n(H+)=0.1mol/L��2L=0.2mol������n(H+)> n(OH-)���кͷ�Ӧ�����������Ϻ�������Һ�����ԣ������Һ��H+Ũ��Ϊ
����n(OH-)=10-2mol/L��9L=0.09mol��pH =1��H2SO4��Һ��c(H+)=0.1mol/L����n(H+)=0.1mol/L��2L=0.2mol������n(H+)> n(OH-)���кͷ�Ӧ�����������Ϻ�������Һ�����ԣ������Һ��H+Ũ��Ϊ![]() ����������ҺpH=2��A����ȷ��
����������ҺpH=2��A����ȷ��
B.��A���֪����a:b=9:2���û����Һ��pH=2���������Һ��H+Ũ��Ϊ0.01mol/L�������Һ���Ϊ(a+b)L��������Һ��H+���ʵ���Ϊ0.01mol/L��(a+b)L=0.01(a+b)mol���ܽ����۵ķ�ӦʽΪFe+2H+=Fe2++H2���������ܽ����۵������� ![]() ��B����ȷ��
��B����ȷ��
C.pH=11��Ba(OH)2��Һ��![]() ����n(OH-)=10-2mol/L��aL=0.01amol��pH =1��H2SO4��Һ��c(H+)=0.1mol/L����n(H+)=0.1mol/L��bL=0.1bmol����ʹ���û����ҺΪ���ԣ���n(H+)= n(OH-)����0.1bmol =0.01amol��a:b=10:1��C�����
����n(OH-)=10-2mol/L��aL=0.01amol��pH =1��H2SO4��Һ��c(H+)=0.1mol/L����n(H+)=0.1mol/L��bL=0.1bmol����ʹ���û����ҺΪ���ԣ���n(H+)= n(OH-)����0.1bmol =0.01amol��a:b=10:1��C�����
D.�����û����ҺΪ���ԣ�����ǰ������H+��Ba(OH)2��OH-���ʵ�����ȣ�ȡΪ0.1bmol�����ǰn(H2SO4)=n[Ba(OH)2]=0.05bmol�����ʱH2SO4 +Ba(OH)2=BaSO4��+2H2O����������BaSO4���������ʵ���Ϊ0.05bmol��D����ȷ����ѡC��


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵��ǣ� ��
����ˮ��������ƽ��Br2��H2O![]() HBr��HBrO����������������Һ����Һ��ɫ��dz
HBr��HBrO����������������Һ����Һ��ɫ��dz
�ڹ�ҵ�ϳɰ���ӦN2(g) ��3H2(g)![]() 2NH3(g) ��H��0��Ϊ��߰��IJ��ʣ�ʵ�������в�ȡ���¡���ѹ�Ĵ�ʩ
2NH3(g) ��H��0��Ϊ��߰��IJ��ʣ�ʵ�������в�ȡ���¡���ѹ�Ĵ�ʩ
�۷�Ӧ2 NO2(g) ![]() N2O4(g)��ƽ�����С���������ʹ��ϵ��ɫ�ȱ�����dz
N2O4(g)��ƽ�����С���������ʹ��ϵ��ɫ�ȱ�����dz
�ܶ���2HI(g) ![]() H2(g) ��I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
H2(g) ��I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
A. �٢� B. �ڢ� C. �ۢ� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֧�Թ��зֱ����������ͬ����ɫ��Һ�������²�����������ȷ����(����)
ѡ�� | ���� | ���� | ���� |
A | �μ�BaCl2��Һ | ���ɰ�ɫ���� | ԭ��Һ����SO42�� |
B | �ȵμ�����ϡ���ᣬ�ٵ���AgNO3��Һ | ��ʼ���������������ɫ���� | ԭ��Һ����Cl�� |
C | �ýྻ��˿պȡ��Һ������ɫ��Ӧ | ����ʻ�ɫ | ԭ��Һ����Na������K�� |
D | �μ�ϡNaOH��Һ����ʪ���ɫʯ����ֽ�����Թܿ� | ��ֽ������ | ԭ��Һ����NH4+ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� CO2 ��һ���������� H2 ��Ӧת��Ϊ�״�(CH3OH)�DZ��Ϊ���ĺð취��һ����������ÿת�� 44 kg CO2 �ų�������Ϊ 49000 kJ��CO2 ת��Ϊ�״�������Ũ����ʱ��ı仯������ͼ��ʾ(��֪��Ӧ����������ڴ������¾�Ϊ����)��������������ȷ����

A. 0��3 min �ڣ��� CO2 �� H2 �������ƽ����Ӧ������ȣ���Ϊ 0.5 mol/(L��min)
B. �˷�Ӧ���Ȼ�ѧ����ʽΪ CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ��H = - 49 kJ/mol
C. �������·�Ӧ��ƽ�ⳣ��K=0.753��1.25/(0.75��0.75)
D. �����¶ȣ��˷�Ӧ��ƽ�ⳣ������Ϊ 0.8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G��һ�ָ߷��ӻ�����������л��ϳɵ��м��壬���������齺��ȡ�����ͨ������;���ϳɣ�

��֪�л���A�к���C��H��O��Cl����Ԫ����ͬһ��̼ԭ���ϲ�ֱ���������������š�
��1��A�Ľṹ��ʽΪ___________��___________����Ӧ�۵ķ�Ӧ����_____________________��
��2�� д����Ӧ�ݺͷ�Ӧ�Ļ�ѧ����ʽ����Ӧ��___________����Ӧ�ޣ���һ�������£�___________��
��3��д��1��E��ͬϵ�������_____________________��д��1����F������ͬ�����ŵ�F��ͬ���칹��Ľṹ��ʽ_______________��
��4�������һ����![]() Ϊԭ�Ϻϳ�
Ϊԭ�Ϻϳ�![]() �ĺϳ�·��__________________�����ϳ�·�߳��õı�ʾ��ʽΪ����
�ĺϳ�·��__________________�����ϳ�·�߳��õı�ʾ��ʽΪ����![]() �ҡ���
�ҡ���![]() Ŀ����
Ŀ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���ε�ȱ������ͨ����ʳ�������������ĵ����(KIO3)������غ͵⻯������Һ���ܷ������з�Ӧ��KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
��1���÷�Ӧ�У���������________������������_____��
��2������3mol I2����ʱ����______mol��ԭ����������
��3������1mol���������뷴Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ_____mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���Ϊ�������л�������Ʒ�ͻ�������ȼ�Ͼ��й�����Ӧ��ǰ����CO2 ����ϳɼ״��Ǻ������� CO2 ����Ч;������ CO2 �Ʊ��״����̿����漰��Ӧ���£�
��Ӧ����CO2(g)��H2(g)![]() CO(g)��H2O(g) ��H1����41.19 kJ��mol-1
CO(g)��H2O(g) ��H1����41.19 kJ��mol-1
��Ӧ����CO(g)��2H2(g)![]() CH3OH(g) ��H2
CH3OH(g) ��H2
��Ӧ����CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g) ��H3����49.58 kJ��mol-1
CH3OH(g)��H2O(g) ��H3����49.58 kJ��mol-1
�ش��������⣺
(1)��Ӧ���� ��S_____����������������������������0����Ӧ���� ��H2��_____��

(2)�ں�ѹ�ܱ������У�����һ������ H2 �� CO2���ٶ���������Ӧ������ʵ���÷�Ӧ���ڲ�ͬ�¶��£���Ӧ��ϵ�� CO2 ��ƽ��ת������ѹǿ�Ĺ�ϵ������ͼ��ʾ��
�ٱȽ�T1��T2 �Ĵ�С��ϵ��T1_____T2 ������ �� �������� �������� ���� ����������_____��
���� T1 �� p6 �������£����ܱ������г��� 3 mol H2 �� 1 mol CO2���÷�Ӧ�ڵ� 5 min ʱ�ﵽƽ�⣬��ʱ���������Ϊ 1.8 L����÷�Ӧ�ڴ��¶��µ�ƽ�ⳣ��Ϊ_____��
a.���������·�Ӧ�� 3 min ʱ�̣��ı��������� A �㴦�ﵽƽ�⣬CH3OH ��Ũ���淴Ӧʱ��ı仯������ͼ��ʾ��3��4 min ��Ũ�ȱ仯δ��ʾ����������ı������Ϊ_____������ H2 ��Ũ�ȱ仯�����4 min ��ʼ��A��ķ�Ӧ����v(H2)=_____(������λС��)��
b.���¶Ȳ��䣬ѹǿ�㶨�� p8 �����������´ﵽƽ��ʱ�������������Ϊ_____L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�����ӷ���ʽ����ȷ����
A. ��Ƭ����NaOH��Һ�������������2Al + 2OH��+ 2H2O===2AlO2��+3H2��
B. ��K2Cr2O7��Һ�еμ�����ŨH2SO4����Һ��ɫ��� Cr2O72��(��ɫ) + H2O![]() 2CrO42��(��ɫ) + 2H+
2CrO42��(��ɫ) + 2H+
C. ��Na2SiO3��Һ��ͨ�����CO2�Ʊ�����������SiO32��+ CO2 + H2O===H2SiO3�����壩+ CO32��
D. ��Na2CO3��Һ���ݹ�¯ˮ������CaSO4����CaSO4 + CO32��![]() CaCO3 + SO42��
CaCO3 + SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С�������50 mL 0.50 mol��L��1�����50 mL 0.55 mol��L��1����������Һ����ͼװ���н����кͷ�Ӧ���Իش��������⣺
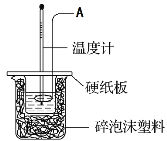
��1������A������__________________________
��2��ʵ����������в�����ȷ��______________(����ĸ)��
A.���¶ȼ�С�Ľ���
B.�ֶ�μ�������������Һ
C.ֻ����һ��ʵ�飬������õ����ݼ����к���
D.�������¶ȼ��ϵ�A��������½���
��3���������������������Һ���ܶȶ���1 g��cm��3����֪�кͷ�Ӧ��������Һ�ı�����c��4.18 J��g��1������1��Ϊ�˼����к��ȣ�ijѧ��ʵ���¼�������£�
ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
���� | ����������Һ | �����Һ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
���ݸ�ѧ����ʵ�����ݼ��㣬��ʵ���õ��к�����H��__________ (�������һλС��)��
��4�����²�������ʹ��õ��к�����H���������ı仯��(����ƫ������ƫС������������)��
����ȡϡ����ʱ������Ͳ��������õ��к�����H��_______________ ��
�����к��Ȳⶨʵ����δ��ˮϴ���¶ȼ��ϵ�����ֱ�Ӳⶨ����¶ȣ���õ��к�����H��_______________��
�����õ�Ũ�ȵĴ����� NaOH ��Һ��Ӧ�����õ��к�����H�� __________����ԭ����____________________________________________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com