
����Ŀ��ij�¶�ʱ����һ���ݻ�Ϊ2L���ܱ������У�X��Y��Z���������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף� 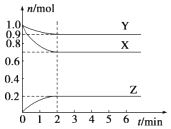
��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2����Ӧ��ʼ��2min������Z�ķ�Ӧ����Ϊ ��
��3����X��Y��Z��Ϊ���壬��Ӧ�ﵽƽ��ʱ��ѹǿ�ǿ�ʼʱ��������ʱ�ų���a kJ����������1���ķ�Ӧ����ʽд���Ȼ�ѧ��Ӧ����ʽʱ���÷�Ӧ�ķ�Ӧ�ȡ�H= ��
��4��ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С���Ժ�����ѧ����ǿ����Ҳ�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ��֪��
��ѧ�� | H��H | H��Cl | Cl��Cl |
����/KJmol��1 | 436 | 431 | 242 |
��ҵ��ͨ�������������г��ȼ����ȡHCl���壬д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ�� ��
���𰸡�
��1��3X+Y?2Z
��2��0.05mol?L��1?min��1
��3��0.90����10akJ?mol��1
��4��H2��g��+Cl2��g��=2HCl��g����H=��184kJ?mol��1
���������⣺����ͼ֪�����ŷ�Ӧ���У�X��Y�����ʵ������٣�Z�����ʵ������ӣ�����X��Y�Ƿ�Ӧ���Z���������1����n��X��=��1.0��0.7��mol=0.3mol����n��Y��=��1.0��0.9��mol=0.1mol����n��Z��=��0.2��0��mol=0.2mol����ͬʱ���ڣ��μӷ�Ӧ�ĸ����ʵ����ʵ����ı仯��֮�ȵ����������֮�ȣ�����X��Y��Z�ļ�����֮��=0.3mol��0.1mol��0.2mol=3��1��2����÷�Ӧ����ʽΪ3X+Y2Z�����Դ��ǣ�3X+Y2Z����2����Ӧ��ʼ��2min��v��Z��= ![]() =
= ![]() =0.05 molL��1min��1 �� ���Դ��ǣ�0.05 molL��1min��1����3���ٿ�ʼʱ���������ʵ���=2.0mol��ƽ��ʱ���������ʵ���=��0.9+0.7+0.2��mol=1.8mol�����º��������£�����ѹǿ֮�ȵ������ʵ���֮�ȣ����Է�Ӧ��ѹǿ�Ƿ�Ӧǰ��
=0.05 molL��1min��1 �� ���Դ��ǣ�0.05 molL��1min��1����3���ٿ�ʼʱ���������ʵ���=2.0mol��ƽ��ʱ���������ʵ���=��0.9+0.7+0.2��mol=1.8mol�����º��������£�����ѹǿ֮�ȵ������ʵ���֮�ȣ����Է�Ӧ��ѹǿ�Ƿ�Ӧǰ�� ![]() =0.9������Ӧ�вμӷ�Ӧ��YΪ0.1mol���ų�akJ����������1molY�μӷ�Ӧ�ų�������ΪakJ��
=0.9������Ӧ�вμӷ�Ӧ��YΪ0.1mol���ų�akJ����������1molY�μӷ�Ӧ�ų�������ΪakJ�� ![]() =10akJ������H=��10a kJmol��1 �� ���Դ��ǣ�0.9����10a kJmol��1����4�������������г��ȼ����ȡHCl���壬��H2��g��+Cl2��g��=2HCl��g����H=436kJmol��1+242 kJmol��1����2��431��kJmol��1=��183kJmol��1 �� ���Դ��ǣ�H2��g��+Cl2��g��=2HCl��g����H=��184kJmol��1 ��
=10akJ������H=��10a kJmol��1 �� ���Դ��ǣ�0.9����10a kJmol��1����4�������������г��ȼ����ȡHCl���壬��H2��g��+Cl2��g��=2HCl��g����H=436kJmol��1+242 kJmol��1����2��431��kJmol��1=��183kJmol��1 �� ���Դ��ǣ�H2��g��+Cl2��g��=2HCl��g����H=��184kJmol��1 ��
�����㾫�������û�ѧƽ��ļ������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ֺ�����ﮡ��ܵ����͵��Ӳ��ϣ������в����ķ��������ɹۣ������е����Խ�����������ʽ���ڣ�����Co2O3��CoO����ʽ���ڣ������������ĵ����˫�棻﮻��������С��ӷ�������ȡ�ߴ�̼������CoCO3)�Ĺ����������£�
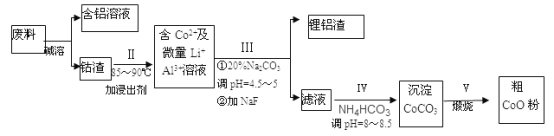
��1������I�в���NaOH��Һ�ܳ������е�Al����Ӧ�����ӷ���ʽΪ_________________________��
��2�����̢��м���ϡH2SO4�ữ���ټ���Na2S2O3��Һ�����ܡ�������ܵ����ӷ�Ӧ����
ʽΪ_____________________(������ֻ��һ�����)��Ҳ����H2SO4��H2O2����H2SO4��Na2S2O3����ô�÷�Ӧ�Ļ�ѧ����ʽΪ______________��������HC1����H2SO4����ɵĺ����______________��
��3�����̢���̼������Һ�������dz���Al3+��Li+��д������Al3+�����ӷ���ʽ___________________��
��4�����̢����ܵ����ӷ���ʽ��______________________��
��5��CoCO3�������Ʊ�����ӵ�ص���������LiCoO2�������������ǽ�n(Li)��n(Co)=l��l��LiCO3��CoCO3�Ĺ��������ڿ����м�����700�桫900�档��д���÷�Ӧ�Ļ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŨH2SO4������������H2��O2�����壬������ŨH2SO4������ ��
A. ��ˮ�� B. ������ C. ���� D. ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A,B,C,D,EΪԭ��������������Ķ���������Ԫ�أ���ԭ�Ӱ뾶�������������Ĺ�ϵ����ͼ1��Eԭ��������ϵĵ�������Dԭ��������������4����D���Ӻ�������Ų���C2����ͬ�� 
�Իش�
��1��Ԫ��E��Ԫ�����ڱ��е�λ���� ��
��2����Ԫ��D��������������������������ͬ������ �� ���û�ѧʽ������ͬ��
��3��B��E����������Ӧ��ˮ������Խ�����Ϊ �� ������ͼ2��װ����֤�������������ǿ��������װ���м�����Լ��ֱ�Ϊ���� �� �� �� �۲쵽��ʵ�������� ��
��4������������Ԫ����ɵ���ѧ���������ʣ�����ɺͽṹ��Ϣ���±���
���� | ��ɺͽṹ��Ϣ |
a | ����A,C,D���� |
b | C,D��ɵĻ������ԭ����֮��Ϊ1��1 |
c | ��ѧ���ΪAC2 |
��a���еĻ�ѧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. úȼ���ǻ�ѧ��ת��Ϊ���ܵĹ���
B. ��Ч��ײ�ǻ�ѧ��Ӧ�����ij�Ҫ����
C. ʯī�Ƚ��ʯ�ȶ�����ʯīת��Ϊ���ʯ�Ƿ��ȷ�Ӧ
D. ij��Ӧ�Ƿ��ȷ�Ӧ��˵���ڳ����¾��ܷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݸ�����Ϣ��д������ԭ����ʽ����9����
��1����֪������������NaClO2�ɷ�����Ӧ����NaCl���ͷų�ClO2���÷�Ӧ�����ӷ���ʽΪ ��
��2��������л�ԭ�ԣ����Ժ�������������Ӧ�������������£�H2S��KMnO4��Ӧ����S��MnSO4��K2SO4��H2O��д���÷�Ӧ�Ļ�ѧ����ʽ��
��3����ʢ��10mL1.0mol��L��1�ĵ�ˮ���Թ��У�ͨ������Cl2��ȫ��Ӧ��ת����0.1mol���ӡ�д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦA (g)+2B(g)![]() 2C (g)������ӦΪ���ȷ�Ӧ���ﵽƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ���ʹA��Ũ������Ӧ��ȡ�Ĵ�ʩ��
2C (g)������ӦΪ���ȷ�Ӧ���ﵽƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ���ʹA��Ũ������Ӧ��ȡ�Ĵ�ʩ��
A. ����ѹǿ B. ����B��Ũ�� C. ����A��Ũ�� D. �����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʳ���䣬��Ϊ�����������( )
A. ��ţ�⡢���ײˡ����ն�������������������ͷ
B. ������ˡ�����˿����ͷ
C. �Ǵ��Źǡ��������㡢��
D. ��ը�����������⡢���⡢��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A,B,C,D,E����ԭ������С��18��Ԫ�أ���������Ϣ���±���
Ԫ�ر�� | ������Ϣ |
A | ��һ��ԭ����ֻ�����ӣ�û������ |
B | L���������K���3�� |
C | ����������B�������Ӿ�����ͬ�ĵ��Ӳ�ṹ���Һ˵������B���3 |
D | �������������ڵ��Ӳ��������ǵؿ��к����϶��Ԫ��֮һ |
E | ����Ϊ����ɫ������������Ư�� |
��ش��������⣺
��1��A��B��C����Ԫ���γɵĻ����ﺬ�еĻ�ѧ�������� ��
��2����A��B��CԪ������������γɵĻ��������Ӧ���ɵ��ʵĻ�ѧ����ʽ�� ��
��3��D������A��E�γɵĻ������ˮ��Һ��Ӧ�����ӷ���ʽ�� ��
��4��д��ʵ������ȡ����E�Ļ�ѧ����ʽ�� ��
��5��C��D��Ԫ���γɵĵ��ʻ����Խ�ǿ���ǣ�дԪ�ط��ţ� �� ����ж������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com