
| A. | 微电池的负极是Mg | B. | 微电池的负极是Al | ||
| C. | 铝的电极反应式为2H++2e-═H2↑ | D. | 镁的电极反应式为Mg-2e-═Mg2+ |
分析 Mg、Al和强碱性溶液构成原电池,铝易失电子而作负极、Mg作正极,负极上电极反应式为Al+4OH--3e-=AlO2-+2H2O,正极上电极反应式为2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-),据此分析.
解答 解:A.该原电池中,铝易失电子作负极,Mg作正极,故A错误;
B,该原电池中,在碱性条件下,铝易失电子而作负极,故B正确;
C.该原电池中,在碱性条件下,铝易失电子而作负极,电极反应式为Al+4OH--3e-=AlO2-+2H2O,故C错误;
D.Mg作正极,电极反应式为2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-),故D错误;
故选B.
点评 本题考查了原电池原理,根据电极上失电子难易程度确定正负极,不能根据金属的活泼性强弱判断正负极,为易错点.


科目:高中化学 来源: 题型:选择题
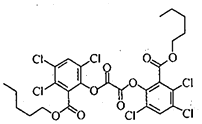 荧光棒的发光原理是利用过氧化氢氧化某草酸二酯产生能量传递给荧光物质发出荧光.该草酸二酯的结构简式如图所示.下列有关该草酸二酯的说法不正确的是( )
荧光棒的发光原理是利用过氧化氢氧化某草酸二酯产生能量传递给荧光物质发出荧光.该草酸二酯的结构简式如图所示.下列有关该草酸二酯的说法不正确的是( )| A. | 分子中含有一种含氧官能团 | |
| B. | 苯环上的一溴代物只有一种 | |
| C. | 可以发生取代反应和加成反应 | |
| D. | lmol草酸二酯与NaOH溶液反应最多消耗4mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了使豆腐白嫩和富有弹性,制作时可使用吊白块(具有漂白性)和烧碱 | |
| B. | 金属Mg失火时不能用泡沫灭火器扑灭 | |
| C. | 土壤胶粒带负电荷,有利于铵态氮肥的吸收 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解过程中OH-向阴极迁移 | |
| B. | 阳极反应式为:4OH--4e-=O2↑+2H2O | |
| C. | 毎有l mol电子转移,生成标准状况下5.6L气体 | |
| D. | 电解过程中阴极区溶液的pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | H2CO3 | HClO |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2×10-12 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3×10-8 |
| A. | lmolCl2通入足量的水中充分反应,转移的电子数约为6.02×1023 | |
| B. | 将少量CO2气体通入NaClO溶液中的离子方程式:CO2+H2O+ClO-═HCO3-+HC1O | |
| C. | 常温下,用蒸馏水不断稀释醋酸,溶液中$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$的值不变 | |
| D. | 向浓度均为1×103 mol/L-1的KC1和K2CrO4混合溶液中滴加1×10-3 mol/L-1的AgNO3溶液Cl-先沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定存在SO42-、SO32-、NH4+,可能存在Na+ | |
| B. | 一定存在SO42-、SO32-、NH4+,一定不存在Cl-、Na+ | |
| C. | 溶液中可能含有Cl-,且Na+浓度至少为0.15mol•L-1 | |
| D. | c(SO42-)=0.1mol•L-1,c(NH4+)<c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
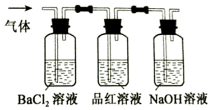 FeSO4受热分解的化学方程式为:2FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+SO2↑+SO3↑
FeSO4受热分解的化学方程式为:2FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+SO2↑+SO3↑查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的氢化物比R的氢化物稳定,沸点高 | |
| B. | Y分别与Z、W、R以两种元素组成的常见化合物有6种 | |
| C. | X与Y形成的两种常见化合物中阴、阳离子的个数比均为l:2 | |
| D. | Z、W、R最高价氧化物对应水化物的酸性由强到弱顺序是:R>W>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com