
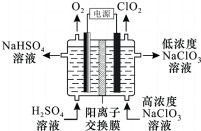
 ClO2是高效杀菌消毒剂.用惰性电极电解NaC1O3溶液制备高纯C1O2的原理如下图所示.下列说法正确的是( )
ClO2是高效杀菌消毒剂.用惰性电极电解NaC1O3溶液制备高纯C1O2的原理如下图所示.下列说法正确的是( )| A. | 电解过程中,Na+向阴极区移动 | |
| B. | 电解产生的O2和ClO2在相同条件下的体积比为1:1 | |
| C. | 阴极的电极反应式是ClO3-+H2O+e-=ClO2↑+2OH- | |
| D. | 电解总反应的化学方程式是4NaClO3+4H2SO4$\frac{\underline{\;电解\;}}{\;}$O2↑+4ClO2↑+4NaHSO4+2H2O |
分析 用惰性电极电解NaC1O3溶液制备高纯C1O2的原理:在阳极上是氢氧根离子失电子的氧化反应4OH--4e-═O2+2H2O,在阴极上是NaClO3得电子的还原反应,8H++4ClO3-+4e-═4ClO2↑+4H2O,电解池中,阳离子移向阴极,根据两极反应式来书写总反应方程式.
解答 解:A、电解过程中,阳离子移向阴极,即Na+向阴极区移动,是部分钠离子移向阴极区,故A错误;
B、在阳极上是氢氧根离子失电子的氧化反应4OH--4e-═O2+2H2O,在阴极上是NaClO3得电子的还原反应,8H++4ClO3-+4e-═4ClO2↑+4H2O,电解产生的O2和ClO2在相同条件下的体积比为1:4,故B错误;
C、阴极的电极反应式是8H++4ClO3-+4e-═4ClO2↑+4H2O,故C错误;
D、在阳极上是氢氧根离子失电子的氧化反应4OH--4e-═O2+2H2O,在阴极上是NaClO3得电子的还原反应,8H++4ClO3-+4e-═4ClO2↑+4H2O,电解总反应的化学方程式是4NaClO3+4H2SO4$\frac{\underline{\;通电\;}}{\;}$O2↑+4ClO2↑+4NaHSO4+2H2O,故D正确.
故选D.
点评 本题考查电解原理,为高频考点,把握电极反应为解答的关键,侧重分析与应用能力的考查,注意电解原理的综合应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
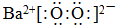 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
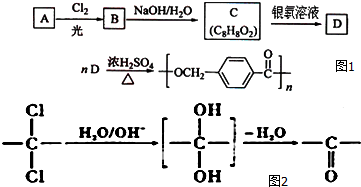
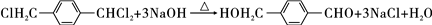 ,该反应过程中生成的不稳定中间体的结构简式应是
,该反应过程中生成的不稳定中间体的结构简式应是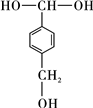 .
.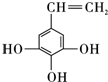 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 室温下,0.2mol•L-1的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是( )
室温下,0.2mol•L-1的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是( )| A. | 溶液可能显中性或酸性 | B. | 升温,c(X)增大,c(Y)减小 | ||
| C. | c(B+)+c(Y)=c(Cl-) | D. | 稀释溶液,c(X)增大,c(Z)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| pH | Ca2+、Mg2+总浓度 | 细菌总数 |
| 6.5~8.5 | <0.004 5mol•L-1? | <100个•mL-1? |
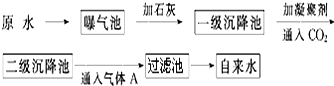
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2可用于加工食品,使食品增白 | |
| B. | NaOH可用于清洗抽油烟机 | |
| C. | 葡萄糖可用于合成保健药物维生素C | |
| D. | 聚丙烯塑料可用作食品保鲜膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
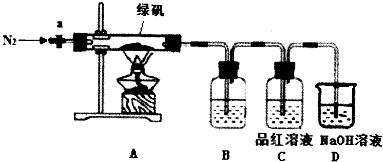
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:e>d | |
| B. | 原子半径:r(e)>r(d) | |
| C. | 最高价氧化物对应水化物的酸性:c<d | |
| D. | a、b可以形成离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com