
【题目】盐酸厄洛替尼是一种治疗肺癌的药物,以芳香化合物A为原料,制备其中间体H的合成路线如下:
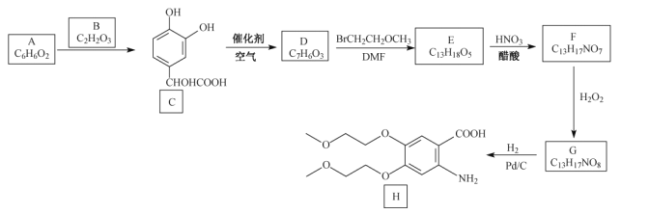
已知:B、D、E、F均能发生银镜反应。
回答下列问题:
(1)A的化学名称__________________。
(2)由A生成C的反应类型为__________________。
(3)B、G的结构简式依次为__________________、__________________。
(4)D生成E的化学方程式为______________________________________________________。
(5)H中含氧官能团名称为_________________。
(6)芳香化合物X是C的同分异构体,写出满足如下条件的X的结构简式:_______________。
①能发生水解反应;②能发生银镜反应;③核磁共振氢谱有四组峰,峰面积之比为3:2:2:1
(7)2-氨基苯乙醚(![]() )可用作染料、香料、医药中间体。请设计以苯酚和乙醇为起始原料制备2-氨基苯乙醚的合成路线____________________________(无机试剂任选)。
)可用作染料、香料、医药中间体。请设计以苯酚和乙醇为起始原料制备2-氨基苯乙醚的合成路线____________________________(无机试剂任选)。
【答案】邻苯二酚(或1,2-苯二酚) 加成反应 ![]()
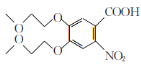
 羧基、醚键
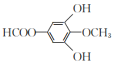
羧基、醚键 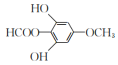 、
、
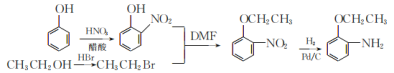
【解析】
A和B反应生成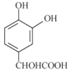 ,结合A的化学式为C6H6O2和B的化学式为C2H2O3及B能发生银镜反应,可知A为
,结合A的化学式为C6H6O2和B的化学式为C2H2O3及B能发生银镜反应,可知A为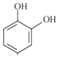 ,B为
,B为![]() ,
, 在空气中催化氧化生成的D化学式为C7H6O3,且能发生银镜反应,则D应为
在空气中催化氧化生成的D化学式为C7H6O3,且能发生银镜反应,则D应为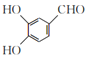 ;G→H是将-NO2还原为-NH2,F→G应该是将-CHO氧化为-COOH,则E→F是发生取代反应,苯环上引入-NO2,结合H的结构简式
;G→H是将-NO2还原为-NH2,F→G应该是将-CHO氧化为-COOH,则E→F是发生取代反应,苯环上引入-NO2,结合H的结构简式 可知,E为
可知,E为 ,F为
,F为 ,G为
,G为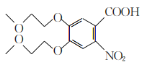 ,据此分析解题。
,据此分析解题。
(1)由分析知A为 ,其化学名称为邻苯二酚(或1,2-苯二酚);
,其化学名称为邻苯二酚(或1,2-苯二酚);
(2)结合A、B和C的化学式的结构可知,由A生成C的反应类型为加成反应;
(3)由分析知:B、G的结构简式依次为![]() 、
、 ;
;
(4) 和BrCH2CH2OCH3发生取代反应生成
和BrCH2CH2OCH3发生取代反应生成 的化学方程式为
的化学方程式为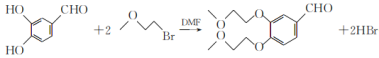 ;
;
(5)H的结构简式为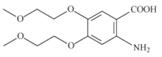 ,结构中含氧官能团名称为羧基、醚键;
,结构中含氧官能团名称为羧基、醚键;
(6)C的结构简式为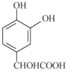 ,其同分异构体X是芳香化合物,说明分子结构中含有苯环,另外:①能发生水解反应,说明含有酯基;②能发生银镜反应,说明含有醛基或甲酸酯基;③核磁共振氢谱有四组峰,峰面积之比为3:2:2:1,则满足条件的X的结构可能是
,其同分异构体X是芳香化合物,说明分子结构中含有苯环,另外:①能发生水解反应,说明含有酯基;②能发生银镜反应,说明含有醛基或甲酸酯基;③核磁共振氢谱有四组峰,峰面积之比为3:2:2:1,则满足条件的X的结构可能是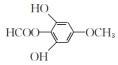 或
或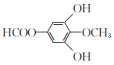 ;
;
(7)2-氨基苯乙醚(![]() )结构中的-NH2,可由硝基还原得到,而苯环上的CH3CH2O-可由苯酚与CH3CH2Br发生取代反应得到,而乙醇与HBr发生取代反应可以得到CH3CH2Br,则苯酚和乙醇为起始原料制备2-氨基苯乙醚的合成路线为
)结构中的-NH2,可由硝基还原得到,而苯环上的CH3CH2O-可由苯酚与CH3CH2Br发生取代反应得到,而乙醇与HBr发生取代反应可以得到CH3CH2Br,则苯酚和乙醇为起始原料制备2-氨基苯乙醚的合成路线为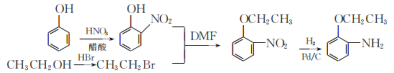 。
。


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组用白云石(主要含CaCO3 和MgCO3)和废铝屑制备一种化合物12CaO·7Al2O3。
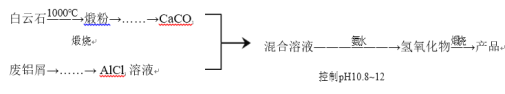
相关信息如下:
①MgCO3 分解温度低于 CaCO3;
②金属离子形成氢氧化物沉淀的 pH 范围:
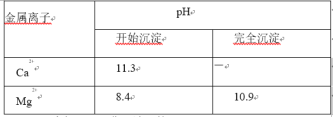
③AlCl3 易水解,易升华。请回答:
(1)从煅粉经一系列操作可制备纯净的CaCO3。请给出合理的操作排序(从下列操作中选取,按先后次序列出字母) :________
煅粉→加入适量 NH4NO3 溶液→( )→( )→( )→通入 NH3 和 CO2,控制pH<11.0→过滤→洗涤→CaCO3
a.过滤 b.控制 pH=11.0 c.控制 pH=8.0 d.取滤渣加水形成悬浊液 e.取滤液
(2)煅粉加入 NH4NO3 溶液发生反应的离子方程式是_________。
(3)通入 NH3 和 CO2 时,需控制 pH<11.0 的原因是_________。
(4)下列说法正确的是_________。
A.煅烧时,需用玻璃棒不断搅拌坩埚中固体,使其受热均匀
B.煅烧时产生 CO2 的体积恰好等于制备 CaCO3 时需要通入 CO2 的体积(已换算为相同状况)
C.NH4NO3 溶液还可用(NH4)2SO4、NH4HCO3 等溶液代替
D.过滤时,应选用玻璃砂漏斗,以免滤纸被溶液腐蚀
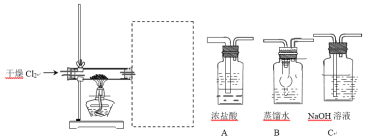
(5)废铝屑需要先放在乙醇和丙酮混合溶液中,放入超声波清洗器中清洗 30 分钟,目的是 __。取出晾干,用以下装置制备 AlCl3 溶液。请为虚线框中补充必须的装置,并按连接顺序排列 ___(填写代表装置的字母,不考虑橡皮管连接)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是
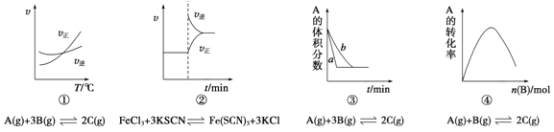
A. ①是其他条件一定时,反应速率随温度变化的图像,则正反应ΔH>0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像
C. ③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图像
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌及其化合物用途广泛。火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有:①2ZnS(s)+3O2(g)=2ZnO(s)+2SO2(g)△H1=﹣930kJmol-1
②2C(s)+O2(g)=2CO(g)△H2=﹣221kJmol-1
③ZnO(s)+CO(g)=Zn(g)+CO2(g)△H3=+198kJmol-1
(1)反应ZnS(s)+C(s)+2O2(g)=Zn(g)+CO2(g)+SO2(g)的△H4=____kJmol-1。
反应中生成的CO2与NH3混合,在一定条件下反应合成尿素:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H。若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是___。
CO(NH2)2(s)+H2O(g) △H。若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是___。
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
c.2v(NH3)正=v(H2O)逆 d.容器中混合气体的密度不再改变
(2)亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在一定条件下合成:2NO(g)+Cl2(g)![]() 2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比[n(NO)/n(Cl2)]进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
2NOCl(g) △H<0。保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比[n(NO)/n(Cl2)]进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
①图中T1、T2的关系为:T1___T2(填“>”、“<”或“=”);
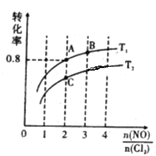
②图中纵坐标为物质___的转化率;
③图中A、B、C三点对应的NOCl体积分数最大的是____(填“A”、“B”、或“C”);
④若容器容积为2L,则B点的平衡常数的值为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种温室气体,对人类的生存环境产生巨大的影响,维持大气中CO2的平衡对生态环境保护有着重要意义。
I.可利用CH4与CO2制备合成气(CO、H2),在某一钢性密闭容器中CH4、CO2的分压分别为15kPa、20kPa,加入Ni/α-A12O3催化剂并加热至1123K使其发生反应:CH4(g)+CO2(g)=2CO(g)+2H2(g)
(1)研究表明CO的生成速率![]() ,某时刻测得p(H2)=10kPa,则该时刻v(CH4)=___________k·Pas-1。
,某时刻测得p(H2)=10kPa,则该时刻v(CH4)=___________k·Pas-1。
(2)达到平衡后,测得CO的产率为50%,则该反应的平衡常数Kp=_________。
(3)科学家提出制备“合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:
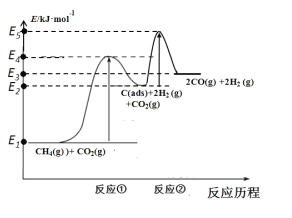
CH4与CO2制备合成气的热化学方程式为__________________。能量变化图中:E5+E1_________E4+E2(填“>”、“<”或“=”)。
II.CO2催化加氢制甲醇5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2,发生以下反应:
i. ![]() ,
,![]()
ii.. ![]()
iii. ![]()
反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如右图所示。
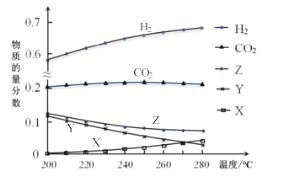
(4)①体系中CO2的物质的量分数受温度的影响不大,原因是_______________________。
②下列措施中,无法提高甲醇平衡产率的是________(填标号)。
A.加入适量CO B.增大压强C.循环利用原料气D.升高温度
③如上图X、Y分别代表_________、________(填化学式)。
III.利用铜基配合物1,10-phenanthroline-Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之,其装置原理如图所示。
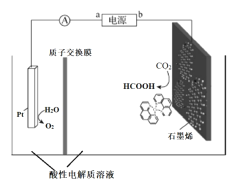
(5)①电池工作过程中,图中Pt电极附近溶液的pH_______(填“变大”或“变小”),阴极的电极反应式为________________。
②每转移2mol电子,阴极室溶液质量增加______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100 ℃的低温下合成一种烃X,此分子的模型如下图(图中的连线表示化学键),下列说法正确的是( )

A. X能使溴的四氯化碳溶液褪色
B. X是一种在常温下能稳定存在的液态烃
C. X分子中在同一平面上的碳原子最多有5个
D. 充分燃烧等质量的X和甲烷,X消耗氧气多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】网络表情包“苯宝宝装纯(醇)”,该分子由“苯宝宝”拿一个氢原子换了个羟基形成,下列说法不正确的是

A. 苯宝宝只想安静地装醇,说明该分子不是醇
B. 该分子中所有原子一定共面
C. 该分子能和Na发生置换反应生成H2
D. 该分子苯环上的一个氢原子被-C4H9取代所得的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
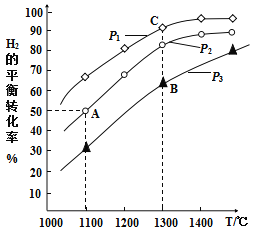
【题目】钼(Mo)是人体及动植物必需的微量元素,且在芯片制作、药物和医学造影等方面也有重要作用。用辉钼矿冶炼金属钼的某反应:MoS2(s)+2Na2CO3(s)+4H2(g)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),该反应中氢气的平衡转化率与温度、压强的关系如图所示:
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),该反应中氢气的平衡转化率与温度、压强的关系如图所示:
(1)Na2S的电子式为:____________。上述反应的气态反应物和生成物中属于极性分子的是____________(填写化学式)。举出一个事实,说明硫的非金属性比碳强(用化学方程式表示)____________。
(2)写出上述反应的平衡常数表达式K=____________。上述正反应是____________反应(填“吸热”或“放热”)。
(3)1100℃,2L恒容密闭容器中,加入0.1molMoS2、0.2molNa2CO3、0.4molH2,反应至20min时达到的平衡状态恰好处于上图中的A点。此过程中,用H2表示的平均速率为____________。其他条件一定时,B点的速率____________C点(填“大于”“等于”或“小于”),说明理由:____________。
(4)A、B、C三点代表的平衡状态的平衡常数的大小为:KA____________KB____________KC(填“大于”“等于”或“小于”),并说明理由:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com