【答案】
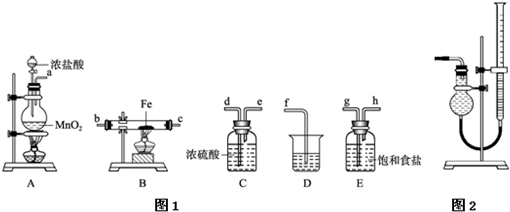
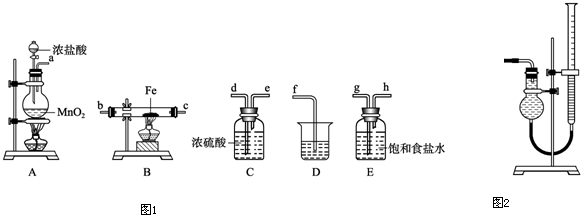
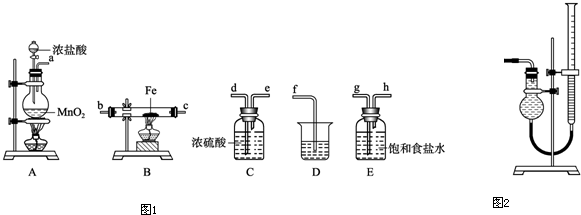
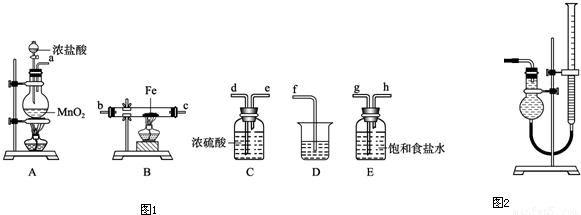
分析:(1)由装置图及药品可知,利用氯气与铁反应制取氯化铁.A中制取氯气,二氧化锰与浓盐酸反应生成氯化锰、氯气、水;
(2)制备氯气中含有氯化氢和水蒸气,除去氯化氢气体用饱和食盐水,除去水蒸气用浓硫酸,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气,防止污染空气;
(3)氯气中含水会导致生成的氯化铁发生水解,得不到纯净的氯化铁;D是吸收多余的氯气防止污染空气;
(4)B中硬质玻璃管内氯气与铁反应生成氯化铁.用KSCN溶液检验Fe
3+,滴加KSCN溶液,溶液变成血红色,说明含有Fe
3+;
(5)①根据滴定管的结构判断;
②Cl
2能溶于水而难溶于饱和食盐水,故应用饱和食盐水,从而提高测量的准确性;
读数时应使圆底烧瓶内外气压相等,故读数前应使左右两边液面相平;
③滴定管内测量前后溶液体积变化为气体体积,俯视时,读取的液面的数值比实际偏小.
解答:解:(1)A中制取氯气,二氧化锰与浓盐酸反应生成氯化锰、氯气、水,反应方程式为4HCl(浓)+MnO
2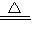
MnCl
2+Cl
2↑+2H
2O,
故答案为:4HCl(浓)+MnO
2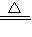
MnCl
2+Cl
2↑+2H
2O;
(2)制备氯气中含有氯化氢和水蒸气,除去氯化氢气体用饱和食盐水,除去水蒸气用浓硫酸,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气,防止污染空气,所以装置顺序为A→E→C→B→D,故答案为:E;C;B.
(3)如果进入B的气体不干燥,FeCl
3容易水解,装置C的作用是干燥Cl
2,防止FeCl
3的水解.D中反应是利用氢氧化钠溶液吸收多余的氯气,反应的离子方程式为:Cl
2+2OH
-=Cl
-+ClO
-+H
2O,故答案为:干燥Cl
2防止FeCl
3的水解;Cl
2+2OH
-=Cl
-+ClO
-+H
2O;
(4)B中硬质玻璃管内氯气与铁反应生成氯化铁,B中因生成有FeCl
3而出现棕(红)色的烟;用KSCN溶液检验Fe
3+,滴加KSCN溶液,溶液变成血红色,说明含有Fe
3+,
故答案为:棕(红)色的烟;硫氰酸钾;
(5)①酸式滴定管下端由活塞,装置中的滴定管没有活塞,应是碱式滴定管,故答案为:碱式;
②Cl
2能溶于水而难溶于饱和食盐水,故应用饱和食盐水,从而提高测量的准确性.应使圆底烧瓶内外气压相等,读数前应上下移动滴定管,使左右两边液面相平,
故答案为:饱和食盐水;上下移动滴定管,使左右两边液面相平;
③俯视时,读取的液面的数值比实际偏小,滴定管内测量前后溶液体积变化偏大,导致所测气体的体积偏大,故答案为:偏大.
点评:本题有一定的综合性,把氯气的实验室制法和氯气的化学性质结合起来.考查学生对实验原理、实验装置的理解、物质的制备与性质,难度中等,(5)③为易错点,注意滴定管内测量前后溶液体积变化为气体体积,滴定管数值由上而下增大.

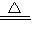 MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O, MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;

 阅读快车系列答案
阅读快车系列答案