
(1)电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则
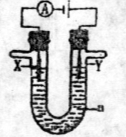
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是 。
②若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中会生成白色固体,发生的总反应化学方程式为
。
该白色固体露置在空气中,可观察到的现象是
。
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为 。通电一段时间后,向所得溶液中加入0.05 mol Cu(OH)2,恰好恢复电解前的浓度和pH,则电解过程中电子转移的物质的量为 mol。高☆考♂资♀源*网
(2)利用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO??4溶液。
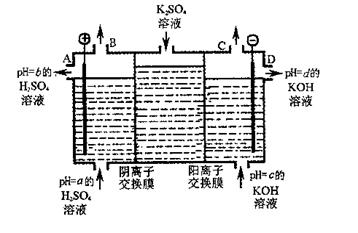
①该电解槽的阳极反应式为 ,通过阴离子交换膜的离子数 (填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为 ;
③电解一段时间后,B口与C口产生气体的质量比为 。
科目:高中化学 来源: 题型:
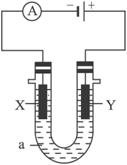
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为________________,在X极附近观察到的现象是______
_______________________;
②Y电极上的电极反应式为________________________,检验该电极反应产物的方法是___
______________________。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是________________________,电极反应式为______________________;
②Y电极的材料是________________________,电极反应式为_______________________。
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)(1)电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是 。
②若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中会生成白色固体,发生的总反应化学方程式为
。
该白色固体露置在空气中,可观察到的现象是
。
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为 。通电一段时间后,向所得溶液中加入0.05 molCu(OH)2,恰好恢复电解前的浓度和pH,则电解过程中电子转移的物质的量为 mol。
(2)利用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液。
①该电解槽的阳极反应式为 ,通过阴离子交换膜的离子数 (填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为 ;
③电解一段时间后,B口与C口产生气体的质量比为 。
查看答案和解析>>
科目:高中化学 来源:2010年云南省高二下学期期末考试化学试题 题型:填空题
(15分)(1)电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则
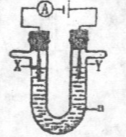
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是 。
②若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中会生成白色固体,发生的总反应化学方程式为
。
该白色固体露置在空气中,可观察到的现象是
。
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为 。通电一段时间后,向所得溶液中加入0.05 mol Cu(OH)2,恰好恢复电解前的浓度和pH,则电解过程中电子转移的物质的量为 mol。
(2)利用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液。
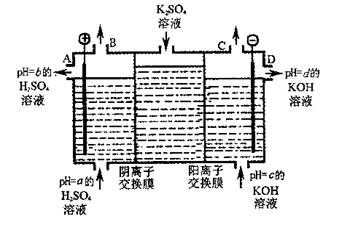
①该电解槽的阳极反应式为 ,通过阴离子交换膜的离子数 (填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为 ;
③电解一段时间后,B口与C口产生气体的质量比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
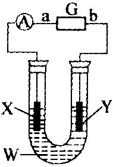
(1)利用电解原理在如图装置中完成粗铜提纯,则电解质溶液W为_________,阳极材料X为_________;
(2)已知直流电源G为高铁电池,高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应式为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH则b电极反应式为_________;放电时每转移3 mol电子,正极有_________mol_________被还原;
3Zn(OH)2+2Fe(OH)3+4KOH则b电极反应式为_________;放电时每转移3 mol电子,正极有_________mol_________被还原;
(3)若X、X为石墨板,W为CuSO4溶液,电解一段时间后,向电解后的残留液中加入足量铁粉充分反应,过滤、蒸干、称重,发现铁粉增重3.2g;洗净、烘干、称重,发现Y板增重1.6 g。则从理论上讲,电解过程中高铁电池的锌电极质量减少_________g;电解后溶液pH为_________;原CuSO4溶液的物质的量浓度为_________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com