
【题目】在一定条件下,反应A2(g)+B2(g)![]() 2AB(g),达到反应限度的标志是( )
2AB(g),达到反应限度的标志是( )
A. 容器内气体的总压强不随时间的变化而变化
B. 单位时间内有nmolA2生成,同时就有nmolB2生成
C. 单位时间内有nmolA2生成,同时就有2nmolAB生成
D. 单位时间内有nmolB2发生反应,同时就有2nmolAB生成
【答案】C
【解析】试题分析:在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。A、反应前后体积不变,所以压强始终是不变的,A错误;B、单位时间内有nmolA2生成,同时就有nmolB2生成均表示逆反应速率,不能说明反应达到平衡状态,B错误;C、单位时间内有nmolA2生成,同时就有2nmolAB生成,其中反应速率的方向是相反的,且满足速率之比是相应的化学计量数之比,可以说明反应达到平衡状态,C正确;D、单位时间内有nmolB2发生反应,同时就有2nmolAB生成均表示正反应速率,所以不能说明是否达到平衡状态,D错误;答案选C。


科目:高中化学 来源: 题型:
【题目】如图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶管的胶头,下列与实验事实不相符的是( )

A. CO2(NaHCO3溶液)无色喷泉
B. NH3(H2O含酚酞)红色喷泉
C. H2S(CuSO4溶液)黑色喷泉
D. HCl(AgNO3溶液)白色喷泉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列生活现象中没有发生化学变化的是
A. 过氧乙酸可用于环境消毒
B. 漂白粉消毒
C. 夜晚霓虹灯放出五颜六色的光
D. 醋除水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法摘自某些刊物,你认为无科学性错误的是
A.铅笔芯的原料是铅,儿童用嘴咬铅笔会导致铅中毒
B.在生有煤炉的居室里放一盆水,可以防止CO中毒
C.在农作物温室大棚内燃烧煤,产生的CO2不利于植物的生长
D.高纯硅应用在半导体元件与集成芯片之中,所以说“硅是信息技术革命的催化剂”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) ![]() 2SO3(g)ΔH<0,某研究小组研 究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g)ΔH<0,某研究小组研 究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
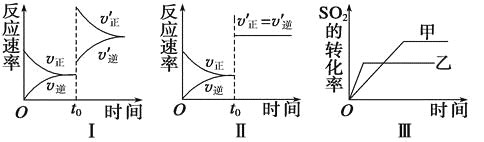
A.图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响
B.图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响
C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙的冷凝管中冷凝水的入口是 (填“a”或“b”),装置己的作用是 ;如何控制两种反应物体积相等: 。
(2)装置戊上方分液漏斗中最好选用下列试剂: (选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 molL1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H ==SO2Cl2 + H2SO4,分离两种产物的方法是______ (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是 (用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有 (写两条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体打火机使用的有机燃料,稍加压降温即可液化,减压(打开阀门)很容易汽化,遇明火燃烧,你认为符合这种条件的有机燃料是
A | B | C | D | |
化学式 | C2H6 | C3H6 | C4H10 | C5H12 |
沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 |
熔点/℃ | -183.3 | -189.7 | -138.4 | -129.7 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
X、Y、Z、Q、R、T是前四周期原子序数依次增大的六种元素,其中X元素形成的气体单质密度最小,Y元素氢化物的水溶液呈碱性,Z、R元素最外层电子数相同且Z的原子序数为R的一半,Q的原子半径在第三周期中最大,T是目前应用最广泛的金属。回答下列问题:
(1)T在周期表中的位置是 ,其M层上的电子排布式为 。
(2)Y、Z、R的第一电离能由大到小的顺序为 (用元素符号表示)。
(3)根据等电子体原理,Y2Z分子的结构式为 。
(4)YZ能被TRZ4溶液吸收生成配合物[T(YZ)(X2Z)5]RZ4,该配合物中含有的化学键类型有 ,RZ42-离子中R原子的杂化方式为 。
(5)由Q与Z、R可形成多种化合物,写出Q2Z2的电子式: ,Q2Z熔点比Q2R高,其原因是 。
(6)QX晶体的结构与NaCl相同,则X-的配位数为 ,若Q+与最邻近X-的核间距离为a pm,阿伏加德罗常数为NA,则QX晶体的密度为 g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ·mol-1。分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硝酸;③稀醋酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是
A. △H1>△H2>△H3
B. △H1>△H2=△H3
C. △H1<△H2<△H3
D. △H1=△H2<△H3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com