
【题目】某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
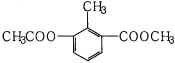
A.一个分子中含有12个H原子
B.苯环上的一氯代物有2种
C.能使酸性KMnO4溶液褪色
D.1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol
 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】下列说法中一定正确的是( )
A.强电解质溶液的导电性比弱电解质溶液的导电性强
B.BaSO4投入水中,导电性较弱,故它是弱电解质
C.弱电解质溶液中存在两种共价化合物分子
D.氯水能导电,所以Cl2是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )

A. 液滴中的Cl―由a区向b区迁移
B. 液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH-
C. 液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈
D. 若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-=Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知三种一元弱酸的酸性强弱:HX>HY>HZ,则相同物质的量浓度的这三种酸的钠盐溶液pH由大到小的顺序正确的是( )
A.NaX、NaY、NaZB.NaZ、NaY、NaX
C.NaY、NaZ、NaXD.NaX、NaZ、NaX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不全是离子化合物的一组是( )
A. 氯化铵、碳酸氢钠、硫酸铝 B. 硝酸钾、火碱、HNO3
C. 氧化镁、食盐、CaCO3 D. K2MnO4、三氧化二铝、硫化钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO、NO2等氮氧化物的消除和再利用有多种方法。
(1)活性炭还原法:某研究小组向某密闭容器中加入足量的活性炭和NO,发生反应:C(s)+2NO(g) N2(g)+ CO2(g) △H = Q kJ·mol-1,在T℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
| 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.40 | 0.20 | 0.30 | 0.30 | |
N2 | 0 | 0.40 | 0.60 | 0.60 | ||
CO2 | 0 | 0.60 | 0.60 |
①0~10min内,N2的平均反应速率v(N2)= ___________ .
②30min后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是 ____ (填序号).
a.加入一定量的活性炭 b.改变反应体系的温度
c.缩小容器的体积 d.通入一定量的NO e.使用催化剂
(2)NH3催化还原法:原理如图所示。

①若烟气中c(NO2) :c(NO)=1 :1,发生图甲所示的脱氮反应时,每转移1.5mol电子放出的热量为113.8kJ,则发生该脱氮反应的热化学方程式为__________________.
②图乙是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为_____________;使用Mn作催化剂时,脱氮率b-a 段呈现如图变化的可能原因是__________(答1点).
(3)直接电解吸收法:先用6%的稀硝酸吸收NOx,生成HNO2(弱酸),再将吸收液导入电解槽中进行电解,使之转化为硝酸,则阳极的电极反应式为________________.
(4)NO2与N2O4之间存在转化:N2O4(g) 2NO2(g),将一定量的N2O4放入恒容密闭容器中。
①己知N2O4的起始压强p0为108 kPa,325℃时,N2O4的平衡转化率为40%,则该温度下反应的平衡常数为:Kp=________kPa(用平衡分压代替平衡浓度计算,分压=总压×各物质的量分数,保留一位小数).
②在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率-压强关系如图所示,在图标出的点中,能表示反应达到平衡状态的点为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从银精矿(其化学成分有Ag、Zn、Cu、Pb、S及SiO2)中提取银、铜和铅的工艺流程如图所示。

(1)步骤①中当盐酸的浓度和KClO3的量一定时,写出两点可提高浸取率的措施:__________________________;步骤②中试剂X为_________(填化学式)。
(2)步骤③中Na2SO3的作用_________(填序号)
a. 氧化剂 b. 还原剂 c. 提供SO32-溶解沉淀 d.水解以提供碱性环境
(3)步骤④滤渣中主要含有两种杂质。为了回收其中有经济效益的非金属单质,某实验小组选择合理试剂,设计实验流程如下,补充完善_________。(已知该单质在碱性溶液中易歧化)

(4)步骤⑤中反应的离子方程式为________________;
(5)粗银可用立式电解精炼。纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是______________________;(答1点)
(6)电解精炼的废水中含有NO3-,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将NO3-还原成无污染气体排放,离子方程式为:_____________;已知25℃,当调节溶液pH=7时,可以将AlO2-的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH- AlO2- +2 H2O的K值________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种可充电锂电池,反应原理是4Li+FeS2 ![]() Fe+2Li2S,LiPF6 是电解质,SO(CH3 )2 是溶剂。下列说法正确的是( )
Fe+2Li2S,LiPF6 是电解质,SO(CH3 )2 是溶剂。下列说法正确的是( )

A. 放电时,a 极被还原
B. 放电时,电解质溶液中 PF6- 向 b 极区迁移
C. 充电时,b 极反应式为Fe+2Li2S-4e-=FeS2+4Li+
D. 充电时,a 极连接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置(加热装置已略去)或操作合理的是( )
|
|
| 盐酸
Na2SiO3溶液 |
A.除去 SO2 气体中的 HCl | B.中和热的测定 | C.吸收氨气 | D.证明碳酸的酸性比硅酸强 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com