
| A. | 三种溶液的pH的大小顺序是①>②>③ | |
| B. | 三种溶液稀释相同倍数,pH变化最大的是① | |
| C. | 三种溶液中含微粒种类多少顺序是:②>①>③ | |
| D. | 三种溶液中由水电离出c(H+)大小顺序是:③>②>① |
分析 A.根据溶液酸碱性判断溶液的pH大小;
B.稀释后①的水解程度、②的电离程度增大,溶液pH变化较小,而③中氢离子的物质的量基本不变,则其pH变化最大;
C.①中含有阳离子多了钠离子,阴离子有亚硫酸根离子、亚硫酸氢根离子,其含有微粒最多,③中不存在HCl分子,则③中微粒种类最少;
D.①促进了水的电离,②③都抑制了水的电离,酸性越强,水的电离程度越小.
解答 解:A.①Na2SO3溶液呈碱性,溶液的pH>7,②CH3COOH溶液呈酸性,氢离子浓度小于0.1mol/L,其pH大于③,③HCl溶液中氢离子浓度0.1mol/L,其pH最小,所以三种溶液的pH的大小顺序是①>②>③,故A正确;
B.三种溶液稀释相同倍数,由于①的水解程度、②的电离程度增大,两溶液的pH变化较小,只有③中氢离子的物质的量基本不变,其pH变化最大,故B错误;
C.①Na2SO3溶液中比②③多了钠离子,还多1种酸根离子,②CH3COOH溶液比③多了弱酸分子,③HCl溶液中含有微粒种类最少,所以三种溶液中含微粒种类多少顺序是:①>②>③,故C错误;
D.①Na2SO3溶液中,亚硫酸根离子水解促进了水的电离,②CH3COOH电离出的氢离子抑制了水的电离,③HCl电离出的氢离子抑制了水的电离,由于浓度相同时③中氢离子浓度较大,则③中水电离的氢离子浓度最小,所以三种溶液中由水电离出c(H+)大小顺序是:①>②>③,故D错误;
故选A.
点评 本题考查了溶液pH的计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握水的电离及其影响,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 CH3COOCH2CH3+H2O;反应类型酯化反应.
CH3COOCH2CH3+H2O;反应类型酯化反应.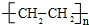 ;反应类型加聚反应.
;反应类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 三种酸的酸性为HX<HY<HZ | |
| B. | 物质的量浓度相同的三种盐的水溶液中,NaZ的溶液中,水的电离程度最大 | |
| C. | pH值相同的三种酸的水溶液,恰好中和时所耗NaOH的物质的量为HX<HY<HZ | |
| D. | 物质的量浓度相同的HZ和NaX能发生HZ+NaX=HX+NaZ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 温度 | 初始pH | 0.1mol/L 草酸溶液/mL | 0.01mol/L KMnO4溶的 体积/mL | 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
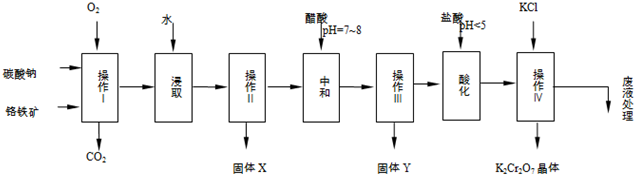
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com