
| A. | BaCl2和H2SO4 | B. | AlCl3和NH3•H2O | C. | NaCl和AgNO3 | D. | Al2(SO4)3和NaOH |
分析 只用试管和胶头滴管就可以对下列各组中的两种溶液进行鉴别,则物质之间添加顺序不同,发生反应产生的现象不同,以此来解答.
解答 解:A.二者反应与量无关,改变滴定顺序均生成硫酸钡白色沉淀,不能鉴别,故A不选;
B.二者反应与量无关,改变滴定顺序均生成氢氧化铝白色沉淀,不能鉴别,故B不选;
C.二者反应与量无关,改变滴定顺序均生成AgCl白色沉淀,不能鉴别,故C不选;
D.NaOH少量时生成白色沉淀,NaOH过量时沉淀消失,反应与量有关,则只用试管和滴管就能鉴别Al2(SO4)3和NaOH,故D选;
故选D.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意与量有关的反应,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述两溶液中盐酸的物质的量浓度比硫酸的物质的量浓度大 | |
| B. | 硫酸使铝钝化 | |
| C. | 生成的氯化铝能溶于水,而生成的硫酸铝难溶于水 | |
| D. | 氯离子可能破坏氧化铝薄膜,而硫酸根离子不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
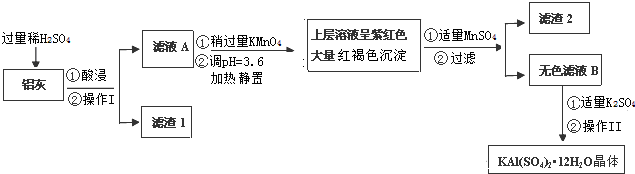
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 7.5 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
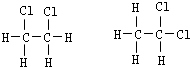 E、
E、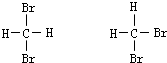
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①②③④ | C. | ②④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al的还原性依次增强 | B. | HF、HCl、H2S的稳定性依次增强 | ||
| C. | H、Li、Na的原子半径依次增大 | D. | KOH、Mg(OH)2、Al(OH)3的碱依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com