
分析 (1)根据化合价的变化和电子转移之间的关系来回答;
(2)由方程式可知,当3molNH3参加反应时,有2molNH3被氧化,根据方程式计算.
解答 解:(1)在KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O反应中,转移5mol电子生成碘单质的量是3mol,所以如果反应中转移0.2mol电子,则生成I2的物质的量为0.12moL,
故答案为:0.12;
(2)由方程式可知,当3molNH3参加反应时,有2molNH3被氧化,消耗Cl21.5mol则
3Cl2+8NH3=6NH4Cl+N2 被氧化NH3
3 2
1.5mol n
$\frac{3}{2}$=$\frac{1.5mol}{n}$,解得n=1mol,
则被氧化的NH3在标准状况下的体积为1mol×22.4L/mol=22.4L,
故答案为:22.4.
点评 本题考查氧化还原的计算,题目难度不大,注意根据反应中元素的化合价的变化分析,本题(2)注意氨气并没有全部被氧化.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素 涤纶 | B. | 麦芽糖 胰岛素 | ||
| C. | 聚乙烯 酚醛树脂 | D. | 淀粉 聚异戊二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入稀硝酸酸化,再滴入BaCl2溶液,产生白色沉淀,则原溶液中一定有SO42- | |
| B. | 向某溶液中加入稀硫酸酸化,再滴入AgNO3溶液,产生白色沉淀,则原溶液中一定有Cl- | |
| C. | 向某溶液中加入碳酸钠溶液,产生白色沉淀,再滴入稀盐酸,沉淀溶解,则原溶液中一定有Ca2+ | |
| D. | 用光洁的铂丝蘸取某无色溶液,在酒精灯外焰里灼烧时观察到黄色火焰,则原溶液中一定有Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
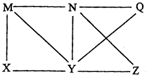 现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )| A. | X可能为Al或Cl2 | B. | Y一定为NaOH(aq) | ||
| C. | N一定是HCl(aq) | D. | Q、Z中的一种必定为Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铅蓄电池的电池总反应式为:
铅蓄电池的电池总反应式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com