
现有四种元素的基态原子的电子排布式如下:
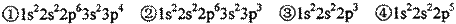
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>① D.最高正化合价:④>③=②>①
科目:高中化学 来源: 题型:
判断集气瓶中是否装满氨气,下列操作中正确的是
A. 在瓶口闻一下是否有刺激性气味 B. 将湿润的红色石蕊试纸放在瓶口
C. 将蘸有浓硫酸的玻璃棒放在瓶口 D. 将蘸有浓盐酸的玻璃棒伸入集气瓶内
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
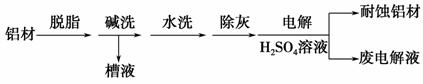
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________________________
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_______________________________________________________。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是_________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_________________________________________________________________。
(3)利用右图装置,可以模拟铁的电化学防护。
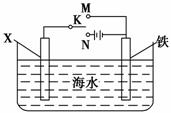
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为______________________________ _____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若不断地升高温度可实现“雪花 水
水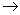 水蒸气
水蒸气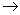 氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是( )
氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是( )
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
1.写出铬原子的基态的核外电子排布式___________________
2.在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有 (填序号),CS2分子的空间构型是_______ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
把3体积NO2气体依次通过①饱和NaHCO3溶液;②浓硫酸;③Na2 O2后(假设每一步的反应都是充分的),再用排水法收集残留气体,则收集到的气体是 ( )。
O2后(假设每一步的反应都是充分的),再用排水法收集残留气体,则收集到的气体是 ( )。
A.1体积NO B.1体积NO 2和
2和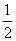 体积O2
体积O2
C.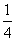 体积O2 D.
体积O2 D.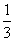
 体积NO
体积NO
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上合成氨的反应原理如下:N2(g)+3H2(g) 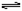 2NH3(g) +Q(Q>0)。
2NH3(g) +Q(Q>0)。
在一密闭容器中进行合成氨反应,一段时间后达到平衡。回答下列问题:
(1)要使H2得到充分利用,可采用的措施是____________;
a.加入氢气 b.升温 c.加压 d.加催化剂
(2)450℃时,往2L密闭容器中充入1 mol N2和2.6 mol H2,反应过程中NH3的物质的量浓度随时间的变化情况如下表所示:
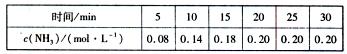
反应开始的5 min内,用消耗氢气表示反应的平均反应速率为 ;
(3)升高温度,v(正)______(填增大、减小或不变),v(逆) ______(填增大、减小或不变),反应混合物中氨气的体积分数________(填增大、减小或不变);
(4)下列叙述中,能说明该合成氨反应已达到平衡的是 (填字母代号)。
A.容器内的气体密度保持不变
B.容器内的气体压强保持不变
C.容器内N2、H2、NH3物质的量浓度之比为1:3:2
D.单位时间内消耗a mol N2,同时生成3a mol H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com