
 ���ж��ֻ���������ᣨH3PO2���ʹ������ƣ�NaH2PO2����Ϊ���������еĻ�ԭ����
���ж��ֻ���������ᣨH3PO2���ʹ������ƣ�NaH2PO2����Ϊ���������еĻ�ԭ����

 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10-6 |
| B��10-10 |
| C��10-8 |
| D��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ʵ��������������������� |
| B��1Ħ����������������NA��O2���ӵ���Է�������֮�� |
| C������٤�����������ǹ涨������û�е�λ |
| D��H2����Է���������1molH2��������H2��Ħ���������ֵ�λ��ͬ������ֵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��Na2S�ĵ���ʽ��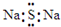 |
B��˳-2-��ϩ�Ľṹ��ʽ�� |
C��O2-�Ľṹʾ��ͼ�� |
| D����ϩ�Ľṹ��ʽ��CH2CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���û�����϶���OԪ�� |
| B����ȷ���Ƿ���OԪ�� |
| C���û������п϶�����̼̼˫�� |
| D���û�����Ľṹֻ��һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1���������������������ҿ������������е��ʷ�Ӧ���磺6Ag��s��+O3��g��=3Ag2O��s����H1
��1���������������������ҿ������������е��ʷ�Ӧ���磺6Ag��s��+O3��g��=3Ag2O��s����H1| ���� |
| Ͷ�ϱ�[n��NO2��/n��CH4��] | 400K | 500K | 600K |
| 1 | 60% | 43% | 28% |
| 2 | 45% | 33% | 20% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʽΪC4H8O�ҿ�������Ʒ�Ӧ�ų��������л������� |
| B������ʽΪC5H10O2����̼�����Ʒ�Ӧ�ų�������̼���л������� |
| C������ʽΪC5H10����ʹ������Ȼ�̼��Һ��ɫ���л������� |
| D��C6H14�зе���ߵ�����������Ӧ��һ�ȴ��л������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʯī | B������KCl |
| C��ϡ���� | D������NaOH |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com