


科目:高中化学 来源: 题型:
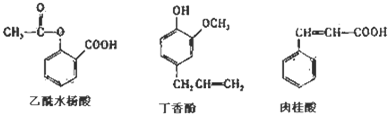
 I:五种短周期元素aA、bB、cC、dD、eE,已知它们的原子序数有如下关系a+b=c,a+c=d,c+d=e,自然界中B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但可以肯定没有第三种元素的化合物种数会超出它们.根据以上信息回答下列有关问题:
I:五种短周期元素aA、bB、cC、dD、eE,已知它们的原子序数有如下关系a+b=c,a+c=d,c+d=e,自然界中B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但可以肯定没有第三种元素的化合物种数会超出它们.根据以上信息回答下列有关问题:

| ||
| 电解 |
| ||
| 电解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:
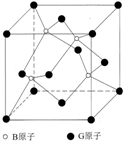 现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)X、Y、Z三种化合物均由短周期元素组成。已知三种化合物的水溶液的焰色反应均呈黄色,Y和Z均由三种元素组成。请根据题目的要求回答下列问题。
(1)固体化合物X为浅黄色粉末,该化合物中含有化学键为 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键
(2)写出X与二氧化碳反应的化学方程式 。
(3)下表为Y和Z实验的部分内容
| 序号 | 主要实验步骤及实验现象 |
| ① | 在Y的无色溶液中,加入稀硫酸,放置。产生浅黄色沉淀和无色有刺激性气味的气体。该气体可使品红溶液褪色。 |
| ② | 在Z的无色溶液中,滴加的盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀。 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到固体。 |
写出含0.1 mol Z的溶液与20 mL 5mol/L的盐酸反应的离子方程式:
实验③加热蒸发、灼烧得到的最终产物主要是 和 。
(4)写出Y与稀硫酸反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com