
【题目】除去下列物质中混有的杂质,选择试剂及操作都正确的一项是( )
选项 | 物质 | 杂质 | 选择试剂 | 实验操作 |
A | Al2O3 | SiO2 | NaOH溶液 | 过滤 |
B | FeCl2 | FeCl3 | Fe粉 | 过滤 |
C | CO2 | SO2 | 澄清石灰水 | 洗气 |
D | I2 | NaCl | 酒精 | 萃取、分液 |
A.A
B.B
C.C
D.D
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】铁不能与冷、热水反应,但能与水蒸气反应。资料显示,在不同温度下,铁粉与水蒸气反应的产物不同,温度低于570 ℃时,生成FeO,高于570 ℃时,生成Fe3O4。某学生用如图所示实验装置,完成还原铁粉与水蒸气反应的实验。

(1)实验中使用肥皂液的作用是____________。
(2)甲同学为探究实验后试管内的固体含有哪些物质,进行 了下列实验:
实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末X放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈绿色;有少量气泡产生 |
② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据上述实验,能确定固体中存在的物质有:______________________________;不能确定是否存在Fe3O4的原因是:___________________________________________。
(3)乙同学设计下列实验方案以确定实验后试管内的固体是否存在Fe3O4。

①溶液X中发生氧化还原反应的离子方程式为___________;
②操作a为_______,检验沉淀是否已经洗涤干净的操作是___________________。
(4)丙同学将试管内固体看做铁的氧化物(FexO),取出6.08 g溶于足量盐酸中,向所得溶液中通入448 mLCl2(标准状况),恰好将Fe2+完全氧化。则x=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl 广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O 制备CuCl,并进行相关探究。
【资料查阅】得知:CuCl常温下是固体,露置于空气中易被氧化为绿色的高价铜盐。CuCl2·2H2O加热分解的情况如右图所示:
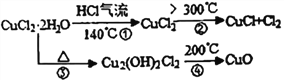
【实验探究】该小组用如图所示装置进行实验(夹持仪器已略)。

根据以上信息请回答下列问题:
(1)装置E的作用是____________________。
(2)实验操作的先后顺序是a→______________________(填操作的编号)
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却 c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热 e.停止通入HCl,然后通入N2
(3)某同学设计的检验该装置气密性的方法是:将装置E上面的倒置漏斗换成导管,在烧杯中加少量水,将导管插入水中,在装置的气体入口处装上橡皮管,并用弹簧夹夹紧,用酒精灯微微加热玻璃管,若导管口有气泡冒出,撤去热源后,导管中有一段稳定的水柱,则装置气密性良好。你认为该同学的设计是否合理________(填“是”或“否”)。
(4)在实验过程中观察到C中纸条的颜色不变,D中纸条的先变红后褪色,其褪色的原因可能是________(填序号)。
A.氯化氢水溶液有漂白性 B.氯气的水溶液有漂白性
C.氯化氢气体有漂白性 D.干燥的氯气有漂白性
(5)停止通入HCl后,通入N2的目的是____________________。
(6)上述CuCl2·2H2O加热分解过程中④中发生反应的化学反应方程式是________________________。
(7)配平工业制备CuCl时发生反应的离子方程式:
Cu2++Cl-+SO32-+H2O→CuCl+H++SO42-,请依次写出配平后的化学计量数__________。
(8)准确称取所制备的氯化亚铜药品mg,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。若滴定结束时,滴定管中有气泡,则样品中CuCl 的质量分数_________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。

(1)写出下列仪器的名称:a.____________,b.___________,e.__________。
(2)仪器a~e中,使用前必须检查是否漏水的有___________。(填序号)
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器是__________,将仪器补充完整后进行实验,温度计水银球的位置在_______处。冷凝水由____口流出(填f或g)。
(4)表示溶液浓度的方法通常有两种;溶液中溶质的质量分数(W)和物质的量浓度 (c),把98%(密度为1.84g/cm3)的浓硫酸稀释成2mol/L的稀硫酸100mL,需要量取浓硫酸_______ mL,若配制时没有冷却到室温就转移、定容,则所配溶液的物质的量浓度________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期埃博拉病毒在非洲各国肆虐,严重威胁了非洲人民的生命。在此期间,环境消毒是极其关键的,常常喷洒一种名为“84”的消毒液,其有效成分为NaClO。下列有关“84”消毒液的说法正确的是
A. “84”的消毒液属于纯净物
B. “84”的消毒液除能杀菌消毒外,还可作漂白剂
C. “84”消毒液中的NaClO比较稳定,不需密封保存
D. “84”消毒液杀菌消毒过程中并未发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)白炭黑(SiO2·H2O)广泛用于橡胶、涂料、印刷等行业,可用蛇纹石[主要成分为Mg6(Si4O10)(OH)8]来制取,其主要工艺流程如下:

(1)蛇纹石用氧化物形式可表示为____________。
(2)碱浸时,为提高其中硅酸盐的浸取率,除采用合适的液固比和循环浸取外,还可采用的方法有①_____________________;②_____________(任举两种)。
(3)过滤1得到的滤液的主要成分是______________________________。
(4)沉淀时加入氯化钠溶液的作用可能是__________________________。
(5)洗涤时,如何证明产品已洗涤干净?_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如下图所示:
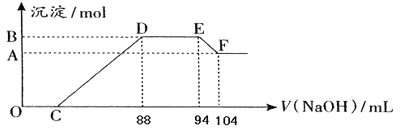
(1)B与A的差值为________mol。
(2)C点对应的溶液体积为________mL。
(3)原硝酸溶液中含硝酸的物质的量为________mol。
(4)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为_______________。
(5)写出铝与该浓度硝酸反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为:5KClO3+6P=3P2O5+5A(已配平)。
(1)生成物A的化学式是_____。
(2)该反应是否是氧化还原反应?_____(填“是”或“不是”)。若是,请指出被还原的元素;若不是,请说明理由:_________。
(3)已知铜在加热时能被浓硫酸溶解,其反应的化学方程式如下:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,用双线桥法表示电子得失的方向和数目:____________。
(4)若2molCu参加反应,则该过程转移的电子是___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究硫酸亚铁的分解产物,将硫酸亚铁装入下图所示的装置a中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是( )

A. 分解的气体产物中有SO3、SO2,应该先检验SO3
B. 装置b中的试剂为Ba(NO3)2溶液,反应后有白色沉淀生成
C. 装置c中的试剂为酸性KMnO4溶液,作用是除去混合气体中的SO2
D. 装置d之后需要增加尾气处理装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com