
【题目】
(1)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示, 该气体所含原子总数为________个,该气体在标准状况下的体积为________L。
(2) 在标准状况下,由CO和CO2组成的混合气体为67.2 L,质量为120 g,此混合物中CO和CO2物质的量之比是________, CO的质量是________,混合气体的平均摩尔质量是 。
(3)若40 g密度为ρ g·cm-3的硝酸钙溶液里含2 g Ca2+,则NO![]() 的物质的量浓度是____________。
的物质的量浓度是____________。
(4)将标准状况下的VL氨气溶于100g水中,得到的氨水密度为ag/cm3,则该溶液的物质的量浓度为 。
(5)标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述:其中正确的是____________
a.体积:②>③>①>④ b.物质的量:②>③>④>①
c.质量:②>③>①>④ d.氢原子个数:①>③>④>②
(6)按体积比为1:2:3所组成的N2、O2、CO2,混合气体20g在标准状况下体积为_________L。
【答案】
(1)![]() NA;
NA;![]() ;
;
(2)1:3;21g;40g/mol;
(3)2.5ρmol·L-1
(4)![]() mol/L;
mol/L;
(5)a、c、d;
(6)12
【解析】
试题分析:(1)mg该气体的物质的量为:n=![]() =
=![]() mol,含有原子的物质的量为:
mol,含有原子的物质的量为:![]() mol×3=
mol×3=![]() mol,该气体所含原子总数为:N=
mol,该气体所含原子总数为:N=![]() mol×NA=
mol×NA=![]() ;在标准状况下的体积为:V=n×22.4L/mol=22.4L/mol×
;在标准状况下的体积为:V=n×22.4L/mol=22.4L/mol×![]() mol=
mol=![]() L,故答案为:
L,故答案为:![]() ;
;![]() ;
;
(2)CO和CO2的总物质的量为![]() =3mol,设CO和CO2的物质的量分别为xmol、ymol,则:x+y=3,28x+44y=120,解得x=0.75、y=2.25,物质的量之比为0.75:2.25=1:3;CO的质量为0.75mol×28g/mol=21g;平均摩尔质量为
=3mol,设CO和CO2的物质的量分别为xmol、ymol,则:x+y=3,28x+44y=120,解得x=0.75、y=2.25,物质的量之比为0.75:2.25=1:3;CO的质量为0.75mol×28g/mol=21g;平均摩尔质量为![]() =40 g/mol,故答案为:1:3;21 g;40g/mol;
=40 g/mol,故答案为:1:3;21 g;40g/mol;
(3)该硝酸钙溶液的体积为:V=![]() =
=![]() =
=![]() cm3,2g钙离子的物质的量为:
cm3,2g钙离子的物质的量为:![]() =
=![]() mol,则该硝酸钙溶液中含有硝酸根离子的物质的量为:
mol,则该硝酸钙溶液中含有硝酸根离子的物质的量为:![]() mol×2=
mol×2=![]() mol,则该溶液中硝酸根离子的物质的量浓度为:c(NO3-)=
mol,则该溶液中硝酸根离子的物质的量浓度为:c(NO3-)=![]() =
= =2.5ρ molL-1,故答案为:2.5ρ mol·L-1;
=2.5ρ molL-1,故答案为:2.5ρ mol·L-1;
(4)溶液的物质的量浓度c=![]() =
=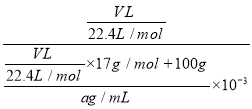 =
=![]() mol/L,故答案为:
mol/L,故答案为:![]() mol/L;
mol/L;
(5)①6.72L CH4的物质的量为![]() =0.3mol,②3.01×1023 个HCl分子的物质的量为
=0.3mol,②3.01×1023 个HCl分子的物质的量为![]() =0.5mol,③13.6g H2S的物质的量为
=0.5mol,③13.6g H2S的物质的量为![]() =0.4mol,④0.2mol NH3。a.根据V=nVm知,相同条件下体积之比等于物质的量之比,故体积④<①<③<②,故a正确;b.由上述计算可知,物质的量为④<①<③<②,故b错误;c.甲烷质量为0.3mol×16g/mol=4.8g,HCl的质量为0.5mol×36.5g/mol=33.25g,氨气的质量为0.2mol×17g/mol=3.4g,故质量④<①<③<②,故c正确;d.甲烷中n(H)=0.3mol×4=1.2mol,HCl中n(H)=0.5mol,硫化氢中n(H)=0.4mol×2=0.8mol,氨气中n(H)=0.2mol×3=0.6mol,故H原子数目②<④<③<①,故d正确;故选a、c、d;
=0.4mol,④0.2mol NH3。a.根据V=nVm知,相同条件下体积之比等于物质的量之比,故体积④<①<③<②,故a正确;b.由上述计算可知,物质的量为④<①<③<②,故b错误;c.甲烷质量为0.3mol×16g/mol=4.8g,HCl的质量为0.5mol×36.5g/mol=33.25g,氨气的质量为0.2mol×17g/mol=3.4g,故质量④<①<③<②,故c正确;d.甲烷中n(H)=0.3mol×4=1.2mol,HCl中n(H)=0.5mol,硫化氢中n(H)=0.4mol×2=0.8mol,氨气中n(H)=0.2mol×3=0.6mol,故H原子数目②<④<③<①,故d正确;故选a、c、d;
(6)体积之比等于物质的量之比,令氮气的物质的量为xmol,则氧气为2xmol,二氧化碳为3xmol,所以:xmol×28g/mol+2xmol×32g/mol+3xmol×44g/mol=20g,解得x=![]() mol,所以标准状况下,混合气体的体积为(
mol,所以标准状况下,混合气体的体积为(![]() mol+2×
mol+2×![]() mol+3×
mol+3×![]() mol)×22.4L/mol=12L,故答案为:12。
mol)×22.4L/mol=12L,故答案为:12。


科目:高中化学 来源: 题型:
【题目】下列哪一个选项中所列的物质均属于动物或植物常利用的能源物质
A. 淀粉糖原纤维素脂肪 B. 淀粉糖原磷脂脂肪
C. 淀粉糖原葡萄糖脂肪 D. 淀粉糖原核糖脂肪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是分离混合物时常用的仪器,回答下列问题:
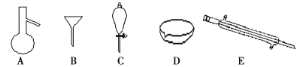
(1)写出上述仪器的名称:A___________,C________________,E________。
(2)分离以下混合物应该主要选用上述什么仪器(填字母)
①粗盐和泥沙:___________;②花生油和水:____________。
(3)关于仪器的使用,下列说法不正确的是________。
A.A仪器可以用酒精灯直接加热
B.B仪器可以用于过滤
C.C仪器在放出液体时应打开上边的塞子
D.在实验室应用D仪器进行实验时要不断用玻璃棒搅拌
E.蒸馏时,E仪器中水的流向是上口进,下口出
(4)若向C装置中加入碘水和足量CCl4,充分振荡后静置,会观察到什么现象?______________。
(5)下列是进行该操作的步骤,正确的顺序是___________。
①将混合物倒入分液漏斗中,并放在铁架台的铁圈上静置,分层;
②从分液漏斗上口倒出上层溶液
③将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接收溶液
⑤检查分液漏斗活塞和颈部的玻璃塞是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,下列有关等质量的二氧化硫气体和二氧化碳气体的叙述中正确的
A.密度比为16:11 B.密度比为11:16
C.体积比为1:l D.体积比为16:11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.![]() 的溶液中:K+、NH4+、SO42-、NO3-
的溶液中:K+、NH4+、SO42-、NO3-
B.0.1 mol/L NaAlO2溶液:Fe3+ 、H+、Cl-、SO42-
C.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
D.使甲基橙试液显黄色的溶液:Fe2+、Mg2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用元素周期律知识解释的是
A. 非金属性:O > S B. 稳定性:HCl >H Br
C. 酸性:HCl > H2CO3 D. 碱性: LiOH <NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
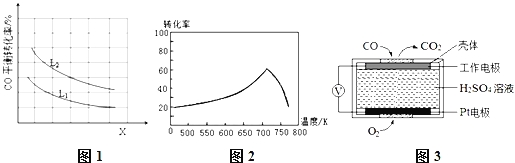
【题目】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品.
(1)CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)![]() COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
①反应0~2min末的平均速率v(COCl2)= mol/(L·min).
②在2min~4min间,v(Cl2)正 v(Cl2)逆 (填“>”、“=”或“<”),该温度下K= .
③已知X、L可分别代表温度或压强,图1表示L一定时,CO的转化率随X的变化关系.
X代表的物理量是 ;a 0 (填“>”,“=”,“<”).
(2)在催化剂作用下NO和CO转化为无毒气体,2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图2所示.温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是 .
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法.其中CO传感器的工作原理如图3所示,则工作电极的反应式为 ;方法2:氧化还原滴定法.用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度.写出NO与H2O2溶液反应的离子方程式 .
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g)![]() CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是 .
CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.汽油、乙烯均为石油分馏产品
B.金属钠在空气中燃烧的火焰呈黄色,是因为生成的Na2O2为淡黄色固体
C.铁丝在Cl2中燃烧有红棕色的烟,是因为生成的FeCl3为红棕色固体
D.煤的气化、液化、干馏和石油的裂化、裂解、催化重整不全是化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com