
下列物质不能由两种单质直接化合生成的是
A.FeS B.FeCl3 C.CuS D. Fe3O4
科目:高中化学 来源: 题型:
下列说法正确的是
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.将含硫酸的废液倒入水槽,用水冲入下水道
C.用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,在容积为1升的甲、乙两个恒容密闭容器中分别充入H2和I2发生可逆反应:H2(g)+I2(g)⇌2HI(g)△H=-14.9kJ/mol,实验时有关数据如表:
| 容器编号 | 起始浓度mol/L | 平衡时的浓度mol/L | 平衡时放出的热量/KJ | |
| I2 | H2 | HI | ||
| 甲 | 0.01 | 0.01 | 0.004 | Q1 |
| 乙 | 0.02 | 0.02 | a | Q2 |
下列判断正确的( )
A.平衡时,乙中颜色更深,a>0.008
B.平衡时,放出的热量:Q1=1/2Q2=0.149kJ
C.该温度下,该反应的平衡常数K=4
D.平衡后,向甲中再充入0.004mol HI气体,再次达到平衡时HI的百分含量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某未知溶液中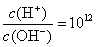 ,且含有大量Al3+和NO
,且含有大量Al3+和NO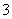 ,检验此溶液中是否大量存在以下6种离子:①SiO
,检验此溶液中是否大量存在以下6种离子:①SiO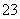 、②NH
、②NH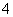 、③Fe2+、④Na+、⑤HCO
、③Fe2+、④Na+、⑤HCO 、⑥Cl-,其中不必检验就能加以否定的离子是:
、⑥Cl-,其中不必检验就能加以否定的离子是:
A.①③⑤ B.②③④ C.①②⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
镁是一种重要的金属资源,工业上制取镁单质主要是电解法。
(1)电解法制取镁单质的反应方程式是:______________________________。
(2)电解原料无水氯化镁可由海水制备。主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩冷却结晶。
其步骤先后顺序是__________________________________;(每步骤可重复使用)
(3)上述步骤①中“一定条件下”具体是指:_______________________________,其目的是___________________________________________。
(4)已知某温度下Mg(OH)2的Ksp=6.4×l0−12,当溶液中c(Mg2+)≤1.0×10−5mol·L−1可视为沉淀完全,则此温度下应保持溶液中c(OH-)≥_________________ mol·L−1。
(5)饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,看到的现象是___________。反应原理可能有两方面,请分别用离子方程式表示:
①________________________________________________;
②________________________________________________。
要验证①②谁是Mg(OH)2溶解的主要原因,可选取________代替NH4Cl溶液作对照实验。
A.NH4NO3 B.(NH4)2SO4 C.CH3COONH4 D.NH4HCO3
(6)镁电池是近年来科学技术研究的热点之一。一种“镁—次氯酸盐”电池的总反应为:
Mg + ClO- + H2O == Mg(OH)2 + Cl- 。其工作时正极的电极反应式:_________________;用此镁电池给铅蓄电池充电,下列说法中正确的是______________________________。
A.镁电池正极与铅蓄电池正极相连
B.电子从Pb电极转移到镁电池负极
C.充电后,铅蓄电池两极质量均减小,理论上镁电池消耗24 g Mg,阴、阳极的质量变化之比为3︰2
D.充电后,镁电池和铅蓄电池的pH均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况,下列反应中属于这种情况的是
①过量的Zn与18 mo1/L硫酸溶液反应;②过量的氢气与少量的氮气在催化剂存在一定条件下充分反应;③过量的水与一定量氯气;④过量的铜与浓硫酸;⑤过量的铜与稀硝酸; ⑥过量的稀硫酸与块状石灰石;⑦常温下过量浓硫酸与铝
A.②③⑤ B.②③④⑥⑦ C.①④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成Z,反应2min后,测得参加反应的X2为0.6mol/L,用Y2变化表示的反应速率v(Y2)= 0.1mol/(L · min),生成的c(Z)= 0.4 mol/L,则该反应方程式为
A.3X2+Y2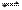 2X3Y B.2X2+Y2
2X3Y B.2X2+Y2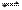 2X2Y
2X2Y
C. X2+2 Y2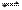 2XY2 D.X2+3Y2
2XY2 D.X2+3Y2 2XY3
2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.足量的硫酸铝溶液与纯碱溶液反应: 2A13++3CO32-+3H2O =2A1(OH)3↓+3CO2↑
B. NaHS溶液的水解方程式: HS-+H2O H3O++S2-
H3O++S2-
C. Fe(OH)3与足量的HI溶液反应: Fe(OH)3+3H+=Fe3++3H2O
D.向亚硫酸氢铵溶液中加入足量的NaOH溶液: NH4++OH-=NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com