
【题目】某有机物是一种医药中间体.其结构简式如图所示.下列有关该物质的说法正确的是( ) 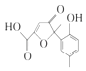
A.该化合物分子中不含手性碳原子
B.该化合物与NaHCO3溶液作用有CO2气体放出
C.1 mol该化合物与足量溴水反应,消耗2 mol Br2
D.在一定条件下,该化合物与HCHO能发生缩聚反应
科目:高中化学 来源: 题型:
【题目】如下图所示的甲、乙、丙三种晶体:

试写出:
(1)甲晶体的化学式(X为阳离子)为________。
(2)乙晶体中A、B、C三种粒子的个数比是________。
(3)丙晶体中每个D周围结合E的个数是________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化镁是一种用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面.镁硅酸盐矿石(主要成分Mg3Si2O5(OH)4 , 含氧化铝、氧化铁、氧化亚铁等杂质)可用于生产氢氧化镁,简要工艺流程如图1: 
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是 .
(2)加入H2O2溶液反应的离子方程式是 .
(3)向溶液Ⅰ中加入的X可以是 , 作用是 .
(4)加入氨水时,Mg2+转化率随温度t的变化如图2所示: ①溶液Ⅱ中发生反应的离子方程式是 .
②t1前Mg2+转化率增大的原因是;
t1后Mg2+转化率下降的原因是(用化学方程式表示) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组溶液混合后,溶液一定呈中性的是( )
A.等体积、等物质的量浓度的氨水与盐酸混合
B.pH之和为14的氨水与硝酸等体积混合
C.pH之和为14的Ba(OH)2溶液与NaHSO4溶液等体积混合
D.等体积、等物质的量浓度的Ca(OH)2溶液与Na2CO3溶液混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验室一般事故的预防和处理方法正确的是
A. 燃着的酒精灯打翻失火,应立即用水浇灭
B. 皮肤上沾有少量浓硫酸,可立即用NaOH冲洗。
C. 少量酸或碱滴到实验台上,立即用湿抹布擦净,再用水冲洗抹布
D. 蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50mol CH4和1.20mol NO2充入体积为1L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是( )
A.T2时CH4的平衡转化率为70.0%
B.该反应的△H>0、T1<T2
C.保持其他条件不变,T1时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O(g),平衡向正反应方向移动
D.保持其他条件不变,T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2 , 与原平衡相比,达新平衡时N2的浓度增大、体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧的含量是衡量水质的一个重要指标,某实验兴趣小组通过如下步骤来测量水中溶解氧的含量: 步骤一:向溶解氧测量瓶中注入20.00mL水样,再分别加入1mL 0.1molL﹣1MnSO4溶液和3mL NaOH和KI的混合溶液,充分反应.此时发生反应的化学方程式为:Mn2++2OH﹣═Mn(OH)2↓ 2Mn(OH)2+O2═2MnO(OH)2
步骤二:向上述混合物中加入1.5mL浓硫酸,充分反应后制沉淀完全溶解,此时溶液呈黄色.
步骤三:将溶液全部转移到容量瓶中,向其中滴加23滴淀粉溶液,溶液呈蓝色.用 0.005molL﹣1的Na2S2O3标准溶液滴定至蓝色恰好消失,共消耗Na2S2O3标准溶液3.60mL.此时发生反应为:I2+2Na2S2O3═2NaI+Na2S4O6
(1)25℃时,步骤一中当加入NaOH使溶液的pH=12时,此时溶液中的c(Mn2+)=molL﹣1 . (已知 KspMn(OH)2=2.06×10﹣13)
(2)写出步骤二中所发生反应的化学方程式:
(3)计算该水样中溶解氧的含量.(单位:mgL﹣1 , 请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别是A,B两种物质的核磁共振氢谱,已知A,B两种物质都是烃类,都含有6个氢原子,试根据两种物质的核磁共振氢谱推测A,B有可能是下面的( ) 
A.A是C3H6 , B是C6H6
B.A是C2H6 , B是C3H6
C.A是C2H6 , B是C6H6
D.A是C3H6 , B是C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳中含量(质量分数)最多的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com