
| A.Ⅰ① | B.Ⅱ② | C.Ⅲ③ | D.Ⅳ④ |
科目:高中化学 来源:不详 题型:填空题
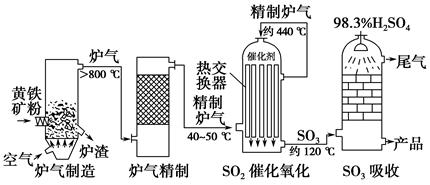
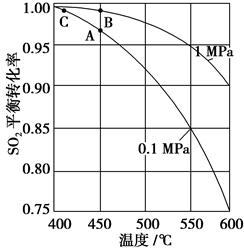
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.立即开启抽油烟机排出煤气,关闭煤气源 |
| B.立即打开电灯,寻找泄漏处 |
| C.立即打开门和窗,关闭煤气源 |
| D.上述三者可同时进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.寻求氮气新来源 |
| B.研制低温下活性较大的催化剂 |
| C.研制500℃左右活性较大的催化剂 |
| D.研制耐高温、高压的新材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸厂不应建在人口稠密的居民区和环保要求高的地区 |
| B.硫酸厂靠近原料产地比靠近硫酸消费中心更为有利 |
| C.硫酸厂生产过程中的污水,含有硫酸等杂质,可用石灰乳中和处理 |
| D.可利用硫酸厂生产过程中产生的“废热”来供热和发电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有少量碳酸氢钙和氯化钙的水是永久硬水 |
| B.明矾有净水作用,所以用明矾处理硬水,可以使硬水软化 |
| C.用离子交换剂处理硬水,可使硬水软化 |
| D.只具有暂时硬度的水经加热煮沸后,可变成软水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2的摩尔质量比Cl2的小 |
| B.Cl2有刺激性气味 |
| C.H2的熔、沸点比Cl2的低 |
| D.H2的溶解度比Cl2的小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com