
| 物质 | Cu(OH)2 | Fe(OH)3 | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.3×10-12 |
分析 (1)加入的物质用于调节pH以除去杂质,主要将铁离子转化为氢氧化铁沉淀,且不能引入新杂质,先根据溶液的pH计算氢离子浓度,再结合水的离子积常数计算氢氧根离子浓度,最后根据c(Fe3+)=$\frac{{K}_{w}[Fe(OH)_{3}]}{{C}^{3}(OH{\;}^{-})}$计算铁离子浓度;
(2)①CuCl2溶液与KI反应实质铜离子氧化碘离子生成生成碘化亚铜沉淀和单质碘;
②淀粉遇到碘变蓝,依据I2+2S2O32-═S4O62-+2I-可知,当Na2S2O3标准溶液刚好将碘全部反应,淀粉由蓝色变成无色,据此解答.
解答 解:(1)为得到纯净的CuCl2•2H2O晶体要除去氯化铁,加入的物质和氯化铁反应生成氢氧化铁且不能引进新的杂质,所以加入物质后应能转化为氯化铜,所以应该加入含铜元素和氢氧根离子的物质,可以是氧化铜、氢氧化铜或碱式碳酸铜;
溶液的pH=4,所以溶液中氢离子浓度为10-4 mol/L,则氢氧根离子浓度为10-10 mol/L,c(Fe3+)=$\frac{{K}_{w}[Fe(OH)_{3}]}{{C}^{3}(OH{\;}^{-})}$=$\frac{2.6×10{\;}^{-39}}{(1×10{\;}^{-10}){\;}^{3}}$=2.6×10-9mol/L;
故答案为:氧化铜或碱式碳酸铜、氢氧化铜;2.6×10-9mol/L;
(2)①CuCl2溶液与KI反应实质铜离子氧化碘离子生成生成碘化亚铜沉淀和单质碘,离子方程式:2Cu2++4I-=2CuI↓+I2;
故答案为:2Cu2++4I-=2CuI↓+I2;
②淀粉遇到碘变蓝,依据I2+2S2O32-═S4O62-+2I-可知,当Na2S2O3标准溶液刚好将碘全部反应,淀粉由蓝色变成无色,所以可以淀粉做指示剂,当淀粉由蓝色变成无色且半分钟不变化滴定达到终点;
故答案为:淀粉; 淀粉由蓝色变成无色且半分钟不变化.
点评 本题考查物质分离提纯,氧化还原滴定测物质的含量,为高频考点,题目难度中等,涉及物质分离和提纯、基本实验操作、滴定实验及计算等知识点,侧重分析与实验能力的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 异戊二烯分子里的所有原子不可能在同一平面上 | |
| B. | 浓氨水洗涤做过银镜反应的试管 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物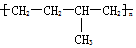 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 厕所清洁剂 厨房清洁剂 醋 肥皂 | |
| B. | 醋 厕所清洁剂 厨房清洁剂 肥皂 | |
| C. | 厕所清洁剂 醋 肥皂 厨房清洁剂 | |
| D. | 厨房清洁剂 厕所清洁剂 肥皂 醋 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

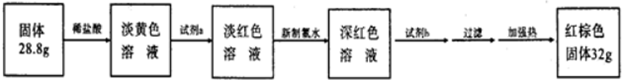
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).
现使用酸碱中和滴定法测定市售白醋的总酸量(g•100mL-1).| 滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
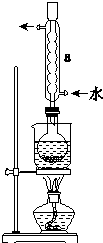 Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
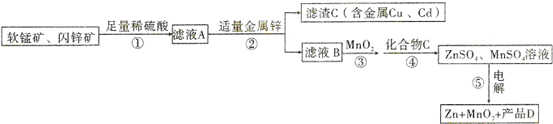
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将待测液NaOH溶液取到锥形瓶后,露置空气中较长时间,以酚酞为指示剂测定 | |
| B. | 以甲基橙为指示剂,当甲基橙变红时停止滴定 | |
| C. | 移液管用蒸馏水冲洗后直接移取待测液 | |
| D. | 滴定终点读数时俯视 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com