
| A、石墨、大理石、胆矾 |
| B、铁矿、小苏打、空气 |
| C、水银、水蒸气、氯水 |
| D、金属钠、食盐水、双氧水 |
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用激光笔照射鸡蛋清水溶液 | 有丁达尔效应 | 鸡蛋清分子直径介于1nm~100nm |
| B | 向某氯化亚铁溶液中滴入少量氯水,然后滴入少量的KSCN溶液 | 溶液变成血红色 | 说明原氯化亚铁已氧化变质 |
| C | 加热分解某盐X,将产生的气体通入硝酸酸化的BaCl2溶液 | 实验开始立即产生白色沉淀 | X可能是NaHCO3 |
| D | 向溶液X中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、催化脱氢反应中NH3BH3作氧化剂 |
| B、NH4BO2和NH3BH3含有的化学键不完全相同 |
| C、0.1 mol NH3BH3发生催化脱氢反应,可以生成6.72 L H2 |
| D、元素N的第一电离能小于元素O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、导致易拉罐变瘪的离子反应是:CO2+OH-=HCO3- |
| B、导致易拉罐又鼓起来的反应是:Al3++3HCO3-=Al(OH)3+3CO2 |
| C、若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
| D、上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
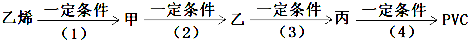
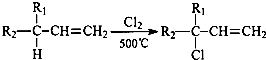
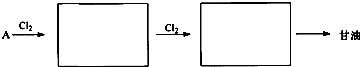
查看答案和解析>>
科目:高中化学 来源: 题型:
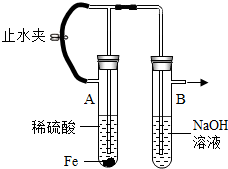 下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )
下图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.关于此实验,下列说法正确的是( )| A、装入药品后应关闭铁夹,等反应完成后再打开铁夹 |
| B、此装置是通过H2的排出使A中压强减小,从而将B中的烧碱吸入A中产生Fe(OH)2 |
| C、H2的作用是排尽装置内的空气和将A中溶液压人B中 |
| D、在药品用量上硫酸应过量,使铁粉能充分反应完 |
查看答案和解析>>
科目:高中化学 来源: 题型:
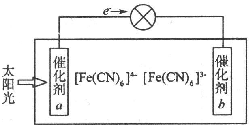 铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题.
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com