
下列说法正确的是( )
A.分子内共价键越强,分子越稳定,其熔沸点也越高
B.C、H、O、N四种元素组成的化合物一定是离子化合物
C.HF分子间存在着氢键,所以HF比HCl稳定
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源:2015-2016学年安徽六安市高二下第三次月考化学试卷(解析版) 题型:选择题
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
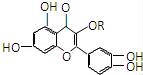
A.可以和溴水反应
B.可以用有机溶剂萃取
C.分子中有三个苯环
D.1 mol 维生素P可以和4 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期6月月考化学试卷(解析版) 题型:实验题
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
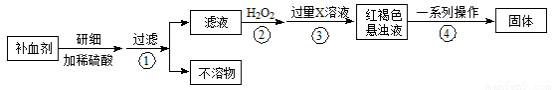
请回答下列问题:
(1)补血剂存放时间较长会氧化变质,对滤液中铁元素的存在形式提出如下假设:
假设1:只有Fe2+
假设2:只有Fe3+
假设3: 。
(2)如何证明步骤①滤液中含有Fe2+ 。
(3)步骤④中一系列处理的操作步骤: 、洗涤、灼烧、 、称量。
(4)该小组有些同学认为可用酸化的KMnO4溶液滴定进行Fe2+含量的测定。
①用离子方程式表示该滴定原理:____________________
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、量筒、药匙、胶头滴管外,还需 。
重复滴定三次,消耗1.00 mol/L KMnO4标准溶液体积分别为19.98 mL、20.00 mL、20.02mL,3次实验所用Fe2+溶液的体积为20.00 mL。请根据以上数据,再设计合理数据,完成下列实验过程的记录表格。(必须填满)
实验编号 | Fe2+溶液的 体积/mL | |||
1 | 20.00 | |||
2 | 20.00 | |||
3 | 20.00 |
③如何判断达到滴定终点:____________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期6月月考化学试卷(解析版) 题型:选择题
下列物质在一定条件下能够导电,但不属于电解质的是( )
A.铝 B.食盐 C.硫酸 D.蔗糖
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上第四次质检化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是( )
A.向稀HNO3中滴加Na2SO3溶液:SO32﹣+2H+=SO2↑+H2O
B.漂白粉溶液中通入足量二氧化硫气体:ClO﹣+SO2+H2O═HClO+HSO3-
C.NaHCO3溶液中加少量Ba(OH)2溶液:HCO3﹣+Ba2++OH﹣═BaCO3↓+H2O
D.向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上第四次质检化学试卷(解析版) 题型:选择题
阿伏加德罗常数约为6.02×1023mol﹣1,下列说法中正确的是( )
A.常温常压下,N2和O2混合气体22.4L所含的分子数少于6.02×1023
B.1L lmol.L﹣1 FeBr2溶液与l mol氯气反应时转移的电子数为3NA
C.标准状况下,11.2L HF所含的分子数约为3.01×1023
D.0.5mol.L﹣1硫酸钠溶液中含有溶质离子总数为1.5NA
查看答案和解析>>
科目:高中化学 来源:2016届广东省广州市高三下4月月考化学试卷(解析版) 题型:选择题
在2L的密闭容器中进行如下反应:CO(g)+H2O(g)?TCO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是( )
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=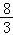
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省运城市高二上学期单元测4化学试卷(解析版) 题型:填空题
氮可以形成多种离子,如N3﹣,NH2﹣,N3﹣,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似
于NH4+,因此有类似于 NH4+的性质.
(1)写出N2H62+在碱性溶液中反应的离子方程式 .
(2)NH2﹣的电子式为 .
(3)N3﹣有 个电子.
(4)写出二种由多个原子组成的含有与N3﹣电子数相同的物质的化学式 .
(5)等电子数的微粒往往具有相似的结构,试预测N3﹣的构型 .
(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”.迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形.如果5个N结合后都达到8电子结构,且含有2个N≡N键.则“N5”分子碎片所带电荷是 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省烟台市高二化学上学期段考试卷(解析版) 题型:选择题
关于化学反应,下列叙述中不正确的是( )
①放热的反应发生时不必加热
②化学反应一定有能量变化
③吸热反应需要加热后才能发生
④化学反应热效应数值(放出或吸收的热量)与参加反应的物质的多少有关.
A.①② B.②③ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com