
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成
HmX分子。在a g HmX中所含质子的物质的量是( )。
A.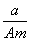 (A-N+m) mol
(A-N+m) mol
B.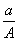 (A-N) mol
(A-N) mol
C.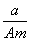 (A-N) mol
(A-N) mol
D.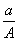 (A-N+m) mol
(A-N+m) mol
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
为了比较铁和铜金属活动性强弱,某研究小组的同学设计了如下一些方案,并将实验结果记录如下:
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| ④将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡,铜片上不产生气泡 |
| ⑤将铁片和铜片同时插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案一共有 ( )。
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)纯净物根据其组成和性质可进行如下分类:
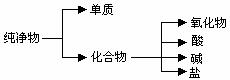
上图所示的分类方法属于 (填序号)
A、交叉分类法 B、树状分类法
(2)写出下列反应的离子方程式:
①Cu(OH)2与盐酸反应
②Ba(OH)2与H2SO4溶液反应
③NaHCO3溶液与盐酸反应
④石灰石与硝酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的原子最外层只有一个电子,它与卤素结合时,所形成的化学键是
( )。
A.一定是离子键
B.一定是共价键
C.可能是离子键,也可能是共价键
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X元素原子的K、L层的电子数之和比L、M层的电子数之和多1个电子。Y元素的原子最外层电子数比内层电子数少3个。Z元素核外有3个电子层,最外层有3个电子。W元素最高化合价是最低化合价绝对值的3倍,它在最高价氧化物中的质量分数为40%。
(1)Y和W的气态氢化物的稳定性为(用化学式表示)________>________。 (2)X单质在空气中加热生成的化合物是________化合物(填“离子”或“共价”)。
(3)X和Z的最高价氧化物对应水化物反应的离子方程式_____________________。
(4)W的低价氧化物与Y单质的水溶液反应的化学方程式________________________
________________________________________________________________________。
(5)Y与Z形成化合物的化学式是________。实验测得当此化合物处于固态和液态时不导电,溶于水能导电。由此判断该化合物具有________(填“离子”或“共价”)化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
A+、B+、C-、D、E五种微粒(分子或离子),它们都分别含有10个电子,已知它们有如下转化关系:
①A++C-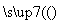 D+E↑
D+E↑
②B++C-―→2D
(1)写出①的离子方程式 ____________________________________________。
写出②的离子方程式_______________________________________________。
(2)除D、E外,请再写出两种含10个电子的分子__________________________
___________________________________ ______________________________。
______________________________。
(3)除A+、B+外,请再写出两种含10个电子的阳离子_____________________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9米(m),其研究成果广泛应用于催化及军事科学中,“纳米材料”是指直径以几纳米到几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是 ( )
A.分散质粒子不能透过滤纸 B.具有丁达尔效应
C.分散质很快就沉降下来 D.所得分散系是溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式:
 XY2(l)+3O2(g) XO2(g)+2YO2(g)。冷却后,在标准状况下测得生成物的体积是672ml,
XY2(l)+3O2(g) XO2(g)+2YO2(g)。冷却后,在标准状况下测得生成物的体积是672ml,
密度是2.56g/L。则:
(1)反应前O2的体积是___________mL;
(2)化合物XY2的摩尔质量是_________;
(3)若XY2分子中X、Y两元素原子的质量比是3:16,则X、Y两种元素分别是________
和_____________(写出元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用密度为1.25 g·mL-1,溶质质量分数为36.5%的浓盐酸配制240 mL 0.1 mol·L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为________。
(2)配制240 mL 0.1 mol·L-1的盐酸
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________。
A.用30 mL水洗涤________2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡、摇匀
E.改用________加水,使溶液凹液面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线________处 (4)操作A中,将洗涤液都移入容量瓶,其目的是___________________________。
(5)若实验过程中出现如下情况如何处理?
①加蒸馏水时不慎超过了刻度线:________。
②向容量瓶中转移溶液时不慎有液滴溅在容量瓶外面:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com