
下列说法正确的是( )
|
| A. | 22.4L氧气中一定含有6.02×1023个氧分子 |
|
| B. | 18g水在标准状况下的体积是22.4L |
|
| C. | 标准状况下,20mL NH3与60mL O2所含的分子数之比为1:3 |
|
| D. | 物质的摩尔质量在数值上等于其相对分子质量或相对分子质量 |
考点:
阿伏加德罗常数;气体摩尔体积.
专题:
阿伏加德罗常数和阿伏加德罗定律.
分析:
A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算氧气的物质的量;
B.水在标准状况下不是气体,不能使用标况下的气体摩尔体积计算水的体积;
C.相同条件下,气体的体积之比=其物质的量之比=分子数之比;
D.当摩尔质量以g/mol为单位时,摩尔质量在数值上等于其相对分子质量或相对分子质量.
解答:
解:A.没有告诉在标况下,不能使用标况下的气体摩尔体积计算22.4L氧气的物质的量,故A错误;
B.18g水的物质的量为1mol,标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算1mol水的体积,故B错误;
C.标准状况下,20mL NH3与60mLO2的物质的量之比等于气体体积之比,为20mL:60mL=1:3,所含的分子数之比为1:3,故C正确;
D.摩尔质量单位如果为kg/mol,则摩尔质量在数值上不等于其相对分子质量或相对分子质量,故D错误;
故选C.
点评:
本题考查阿伏加德罗常数的有关计算和判断、摩尔质量与相对原子量的关系,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件.


科目:高中化学 来源: 题型:
通常状况下,X、Y和Z是三种气态单质。X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I-+2H+ I2+Z+H2O常作为Y的鉴定反应。
I2+Z+H2O常作为Y的鉴定反应。
(1)Y与Z的关系是(选填字母)_______。
a.同位素 b.同系物 c.同素异形体 d.同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法_________________________________________________________________
___________________________________________________________________。
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示)。
___________________________________________________________________。
(4)气体(CN)2与X化学性质相似,也能与H2反应生成HCN(其水溶液是一种酸)。
①HCN分子中含有4个共价键,其结构式是__________________________________。
②KCN溶液显碱性,原因是(用离子方程式表示)_____________________________。
(5)加热条件下,足量的Z与某金属M的盐MCR3(C为碳元素)完全反应生成CR2和MmRn(m、n均为正整数)。若CR2质量为 1g,MmRn质量为
1g,MmRn质量为 2g,M的相对原子质量为a,则MmRn中m:n=_____________(用含
2g,M的相对原子质量为a,则MmRn中m:n=_____________(用含 和a的代数式表示)。
和a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
脱除天然气中的硫化氢既能减少环境污染,又可回收硫资源。
(1)硫化氢与FeCl3溶液反应生成单质硫,其离子方程式为 。
(2)用过量NaOH溶液吸收硫化氢后,以石墨作电极电解该溶液可回收硫,其电解总反应方程式(忽略氧的氧化还原)为 ;该方法的优点是 。
(3)一定温度下1 mol NH4 HS固体在定容真空容器中可部分分解为硫化氢和氨气。
①当反应达平衡时ρ氨气×p硫化氢=a(Pa2),则容器中的总压为 Pa;
②下图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平 衡,请在图上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线.
衡,请在图上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线.

查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组进行与NH3有关的系列实验。
⑴从下图中挑选所需仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。
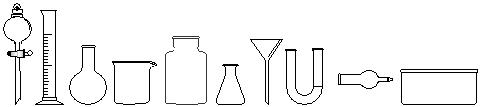
⑵将NH3通入溴水中,有N2生成,反应的化学方程式为 。
⑶为验证“同温同压下,相同体积的任何气体都含有相同数目的分子”,该小组同学设计了如图所示的装置,图中B管的容积是A管的2倍,活塞K1、K2、K3、K4、K5均(固定装置和尾气处理装置略;HCl和NH3均不溶于石蜡油,也不与之反应;装置气密性好)。
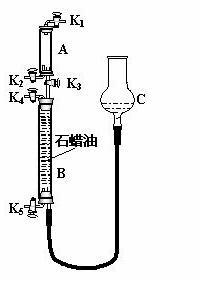
①在A管中充满与大气压强相等的干燥HCl气体。操作是 。
控制活塞K4、K5,调节C,使B管充满与A管同压的干燥NH3。
②缓缓开启K3,A管中的现象是 。要达到实验目的,当反应完成并恢复到室温时,B管中预期的现象是 ;若观察不到预期现象,主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z都是短周期的元素,它们的原子序数依次递增。X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的三倍,Y和Z可以形成两种以上气态化合物,则
(1)X是 ,Y是 ,Z是  。
。
(2)由Y和Z组成,且Y和Z的质量比为7:20的化合物的化学式(分子式)是 。
(3)由X、Y、Z中的两种元素组成,且与X2Z分 子具有相同电子数的两种离子是 和 。
子具有相同电子数的两种离子是 和 。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4:2:3,该盐的化学式(分子式)是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
配制一定体积、一定物质的量浓度的溶液时,下列会使配得的溶液浓度偏低的是( )
|
| A. | 容量瓶中原有少量蒸馏水 |
|
| B. | 溶液从烧杯转移到容量瓶中后没有洗涤烧杯和玻璃棒 |
|
| C. | 定容时观察液面俯视 |
|
| D. | 定容时平视液面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用特殊方法把固体物质加工到纳米级(1nm﹣100nm)的超细粉末粒子,然后制得纳米材料.下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是( )
|
| A. | 溶液 | B. | 悬浊液 | C. | 胶体 | D. | 乳浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,不属于氧化还原反应的是( )
|
| A. | 3Cl2+6KOH=5KCl+KClO3+3H2O |
|
| B. | 2NO2+2NaOH=NaNO3+NaNO2+H2O |
|
| C. | CaO+H2O=Ca(OH)2 |
|
| D. | 2Na2O2+2H2O=4NaOH+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
为提纯下列物质(括号内的物质为为杂质),所选用的除杂试剂和分离方法都正确的是( )
| 被提纯物质 | 除杂试剂 | 分离方法 | |
| A | 苯(苯甲酸) | 生石灰 | 蒸馏 |
| B | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| C | 乙烷(乙炔) | 酸性高锰酸钾溶液 | 洗气 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com