
某稀溶液中含有4 mol KNO3和2.5 mol H2SO4 ,向其中加入1.5 mol Fe,充分反应(已知NO3- 被还原为NO)。下列说法正确的是
A.反应后生成NO的体积为28 L
B.所得溶液中的溶质只有FeSO4
C.所得溶液中c(NO3- )=2.75 mol·L-1
D.所得溶液中c(Fe2+):c(Fe3+ )=1:1
 互动英语系列答案
互动英语系列答案科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
(B)分子式为C6H12O2,属于乙酸乙酯同系物的同分异构体共有
A.12种 B.16种 C.20种 D.24种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三二模考试理综化学试卷(解析版) 题型:简答题
(13分)硫、碳、氮等元素及其化合物与人类的生产生活密切相关,其中.硫酸、氨气、硝酸都是重要的化工原料.而SO2、NO、NO2、CO等相应氧化物又是主要的环境污染物:
(1)过度排放CO2会造成“温室效应”,而煤的气化是高效、清洁利用煤炭的重要途径。煤综合利用的一种途径如图所示。
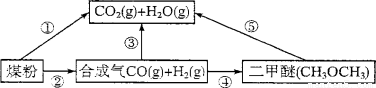
已知:C(s)+H2O(g)=CO(g)+H2(g) AH1= +131.3 kJ·mol-
C(s)十2H2O(g)=CO2(g)+2H2(g) AH2= +90 kJ·mol-
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是 。
(2)298 K时.将氨气放入体积固定的密闭容器中使其发生分解反应。当反应达到平衡状态后.改变其中一个条件X,Y随X的变化符合图中曲线的是 (填字号):

a.当X表示温度时,Y表示氨气的物质的量
b.当X表示压强时.Y表示氨气的转化率
c.当X表示反应时间时.Y表示混合气体的密度
d.当x表示氨气的物质的量时.Y表示某一生成物的物质的量
(3)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染.必须经脱除达标后才能排放:能作脱除剂的物质很多.下列说法正确的是 (填序号):
a.用H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
d.用尿素[CO(NH2)2]作脱除剂.在一定条件下能有效将NOx氧化为N2
(4)在压强为O.1 MPa条件下,容积为V L的密闭容器中,amol CO与2amol H2在催化剂作用下反应生成甲醇。反应的化学方程式为CO(g)+2H2(g)  CH3OH(g),CO的平衡转比率与温度、压强的关系如图所示,则:
CH3OH(g),CO的平衡转比率与温度、压强的关系如图所示,则:
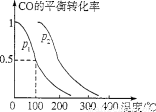
①P1 P2(填“>”“<”或“=”)。
②在其他条件不变的情况下,向容器中增加a molCO与2amol H2.达到新平衡时.CO的转化率 (填“增大””减小”或“不变”.下同),平衡常数 .
③在P1下、100℃时,CH3OH(g)  CO(g)十2H2(g)的平衡常数为 (用含a、V的代数式表示)。
CO(g)十2H2(g)的平衡常数为 (用含a、V的代数式表示)。
(5)①常温下.若将2 mol NH3(g)和l mol CO2(g)通入1 L水中.可得pH=10的溶液,则该溶液中浓度最大的阴离子是 ;
②常温下,将0.01 mol·L- NaOH溶液和0.01 mol·L-(NH4)2SO4溶液等体积混合.所得溶液pH为10,那么该混合液中c(Na+)+c(NH4+)= mol·L一(填准确代数式.不能估算)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:选择题
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:

已知转化过程中的反应为 。
。
转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到平衡状态
B.若用绿矾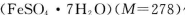 作还原剂,处理1L废水,至少需要917.4 g
作还原剂,处理1L废水,至少需要917.4 g
C.常温下转化反应的平衡常数K=l×10.则转化后所得溶液的pH=6
D.常温下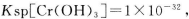 ,要使处理后废水中的c(Cr3+)降至1×10
,要使处理后废水中的c(Cr3+)降至1×10 mol/L,应调溶液的pH=5
mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:填空题
【化学选修3-物质结构与性质】(15分)a、b、c、d、e均为周期表前四周期元素,原子序数依次增大,相关信息如下表所示。
a | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
b | 基基态原子的P轨道电子数比s轨道电子数少1 |
c | 在周期表所列元素中电负性最大 |
d | 位于周期表中第4纵行 |
e | 基态原子M层全充满,N层只有一个电子 |
请回答:
(1)d属于________区的元素,其基态原子的价电子排布图为_________。
(2)b与其同周期相邻元素第一电离能由大到小的顺序为________(用元素符号表示)。
(3)c的氢化物水溶液中存在的氢键有________种,任意画出一种_________。
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为________(用化学式表示)。若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,则A的空间构型为________;A的中心原子的轨道杂化类型为________;与A互为等电子体的一种分子为________(填化学式)。
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为________,若该晶体的相对分子质量为M,密度为ag/cm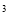 ,则晶胞的体积为________(
,则晶胞的体积为________(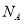 用表示阿伏加德罗常数的值)。
用表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.乙烯使溴水或酸性高猛酸钾溶液褪色均属于加成反应
B.乙醇与浓硫酸混合,加热至170 ℃制乙烯的反应属于取代反应
C.用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应
D.等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三4月阶段测试理综试卷化学试卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,则下列说法正确的是

A.图中甲池为原电池装置,Cu电极发生还原反应
B.实验过程中,甲池左侧烧杯中NO3-的浓度不变
C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液
D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1.01×105 Pa、298K条件下,2mol H2燃烧生成水蒸气时放出484kJ热量.下列热化学方程式中正确的是()
A. H2O(g)═H2(g)+ O2(g)△H=+242 kJ•mol﹣1
O2(g)△H=+242 kJ•mol﹣1
B. 2H2(g)+O2(g)=2H2O(l)△H=﹣484 kJ•mol﹣1
C. H2O(g)+ O2(g)=H2O(g)△H=+242 kJ•mol﹣1
O2(g)=H2O(g)△H=+242 kJ•mol﹣1
D. 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ•mol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com