
有一化学平衡:mA(g)+nB(g) pC(g)+qD(g)(如下图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
pC(g)+qD(g)(如下图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是

A.正反应吸热:m+n>p+q B.正反应吸热:m+n<p+q
C.正反应放热:m+n>p+q D.正反应放热:m+n<p+q
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
在一定温度下,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达到平衡的标志的是( )
2C(g)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等;
②单位时间内有amolA生成的同时生成3amolB;
③A、B、C的浓度不再变化;
④容积不变的密闭容器中混合气体的总压强不再变化;
⑤混合气体的物质的量不再变化;
⑥单位时间消耗amolA,同时生成3amolB ;
⑦A、B、C的分子数目之比为1:3:2。
A.②⑤ B.②⑦ C.①③ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列说法不正确的是
A.对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变 值大于HX溶液的pH改变值
值大于HX溶液的pH改变值
B.在NH3·H2O和NH4Cl浓度均为0.1 mol·L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变
C.在NaH2PO4水溶液中存在关系:c(H3PO4) + c(H+) = c(HPO42-) + c(PO43-) + c(OH-)
D.沉淀溶解平衡AgI 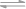 Ag+ + I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质
Ag+ + I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
B.高压比常压有利于由SO2和氧气合成SO3的反应
C.红棕色的NO2,加压后颜色先变深后变浅
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:选择题
反应A(?)+aB(g) C(g)+2D(g)(a为正整数)。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示,下列说法错误的是
C(g)+2D(g)(a为正整数)。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示,下列说法错误的是

A.若a=2,则A为液态或固体
B.该反应的正反应为放热反应
C.T2>T1,p2>p1
D.其它条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一上第一次月考化学试卷(解析版) 题型:选择题
由CO2、H2和CO组成的混合气体在同温、同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为( )
A.19∶8∶13 B.22∶1∶14 C.13∶9∶29 D.26∶16∶27
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:填空题
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g)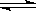 2NH3(g)
2NH3(g) 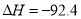 kJ·mol
kJ·mol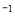 )
)
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
请写出下列物理量的关系:
(1)浓度c1与c2__________________2c2与c3 ________________
(2)能量a与b __________________2b与c___________________
(3)压强p1与p2_________________2p2与p3 __________________
(4)转化率α1与α2_________________α2与α3___________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.强电解质溶液一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在电解质分子
C.强电解质都是离子化合物,弱电解质都是共价化合物
D.不同的弱电解质只要物质的量浓度相同,电离程度也就相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:选择题
在可逆反应2A(g)+3B(g) xC(g)+D(g)中,已知起始浓度A为5 mol/L,B为3 mol/L,C的反应速率为0.5 mol/(L·min),2 min后,测得D的浓度为0.5 mol/L。则关于此反应的下列说法中正确的是( )
xC(g)+D(g)中,已知起始浓度A为5 mol/L,B为3 mol/L,C的反应速率为0.5 mol/(L·min),2 min后,测得D的浓度为0.5 mol/L。则关于此反应的下列说法中正确的是( )
A.2 min末时,A和B的浓度之比为5∶3
B.x=1
C.2 min末时,B的浓度为1.5 mol/L
D.2 min末时,A的消耗浓度为0.5 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com