
| A. | 0.01 mol•L-1的碳酸钠溶液 | B. | pH=12的Ba(OH)2溶液中 | ||
| C. | 0.01 mol•L-1的醋酸 | D. | 0.01 mol•L-1的盐酸 |
分析 根据水电离出的c(H+)=1×10-12 mol/L,水的电离受到抑制,该溶液可能为酸或碱或盐的溶液;据此选择即可.
解答 解:A.由水电离出氢离子的浓度为1×10-12 mol•L-1,水的电离受到抑制,碳酸钠溶液中水的电离受到促进,故A选;
B.由水电离出氢离子的浓度为1×10-12 mol•L-1,水的电离受到抑制,可能为强碱溶液,此时氢离子浓度等于1×10-12,pH=12,可能是pH=12的Ba(OH)2溶液,故B不选;
C.0.01 mol•L-1的醋酸,醋酸电离的氢离子浓度小于0.01 mol•L-1,则水电离出的c(H+)大于1×10-12mol•L-1,故C选;
D.0.01 mol•L-1的盐酸,HCl电离的氢离子浓度等于0.01 mol•L-1,则水电离出的c(H+)=1×10-12mol•L-1,故D不选;
故选AC.
点评 本题考查了pH的有关计算,注意水电离出的氢离子浓度为1×10-12mol/L的溶液,则溶液可能为酸或碱或盐的溶液,明确由水电离出的氢离子浓度及利用该信息来分析问题是解答的关键,难度较小.


科目:高中化学 来源: 题型:选择题
| A. | 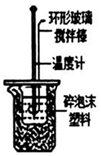 用图所示装置测定中和反应的反应热 | |
| B. |  用图所示装置在实验室制取少置乙烯 | |
| C. | 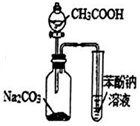 用图3所示装置证明碳酸酸性强于苯酚 | |
| D. | 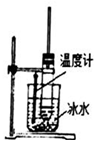 用图所示装置在实验室制取少量硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 混合物 | 化合物 | 单质 | 盐 | |
| A | 盐酸溶液 | NaOH溶液 | 石墨 | 食盐 |
| B | 水玻璃 | KNO3晶体 | O2 | 纯碱(Na2CO3) |
| C | 空气 | 澄清石灰水 | 铁 | 石灰石 |
| D | CuSO4•5H2O | CaCl2 | 水银 | CaO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 地壳中含量最高的非金属元素 |
| Y | M层比K层多1个电子 |
| Z | 最外层电子数为内层电子数的0.6倍 |
| W | 与氯形成的氯化物是生活中常用的调味品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
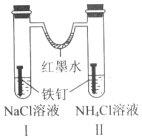
| A. | 红墨水水柱两边的液面变为左低右高 | |
| B. | I 和Ⅱ中负极反应式均为 Fe-2e-=Fe2+ | |
| C. | I 中正极反应式为 O2+2H2O+4e-=4OH | |
| D. | Ⅱ中 NH4Cl 溶液里有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 除去CO2中的HCl气体 | 除去苯中的苯酚 | 观察铁的吸氧腐蚀 | 检验乙炔的还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  该反应过程中的能量变化如图所示 | |
| B. | 该反应条件下,Al的还原性强于Fe | |
| C. | 反应中每生成1 mol Fe转移6×6.02×1023个电子 | |
| D. | 实验室进行该反应时常加入KClO3作催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O?Cl2↑+H2↑+2OH- | |
| B. | 向氯化铝溶液中滴加少量Na2CO3溶液:2Al3++3CO32-?Al2(CO3)3↓ | |
| C. | 一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O | |
| D. | FeCl3溶液与NaAlO2溶液混合:Fe3++3AlO2-?Fe(AlO2)3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com