
已知:
Cu (s)+2H+ (aq)=Cu2+(aq)+ H2 (g) △H 1
2H2O2(l)=2H2O(l) + O2 (g) △H 2
2H2 (g) + O2 (g)=2H2O(l) △H 3
则反应 Cu (s)+H2O2(l)+2H+ (aq)=Cu2+(aq)+ 2H2O(l) 的△H是
A.△H=△H 1+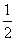 △H 2+
△H 2+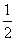 △H 3 B.△H=△H 1+
△H 3 B.△H=△H 1+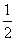 △H 2-
△H 2-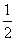 △H 3
△H 3
C.△H=△H 1+2△H 2+2△H 3 D.△H=2△H 1+△H 2+△H 3
科目:高中化学 来源: 题型:
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
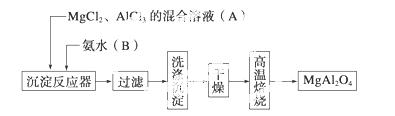
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入________(填“A”或“B”),再滴加另一反应物。
(2)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
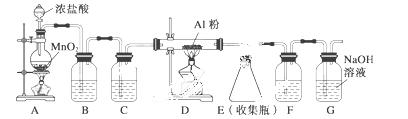
装置B中盛放饱和NaCl溶液,该装置的主要作用是______________。F中试剂的作用是________________。用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)钠镁铝三种元素中第一电离能最大的是 。
(2)某正二价阳离子核外电子排布式为[Ar]3d54s0,该金属的元素符号为 。
(3)微粒间存在非极性键、配位键、氢键及范德华力的是 。
A. NH4Cl晶体 B. Na3AlF6晶体 C. Na2CO3•10H2O晶体
D. CuSO4溶液 E. CH3COOH溶液
(4)部分共价键键能数据如下表:
| 键 | H-H | N-H | N-N | N=N | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 159 | 418 | 945 |
根据上表数据推算并写出由氮气和氢气合成氨气的热化学方程式: 。
(5)乙醇和乙醚是同分异构体,但它们性质存在差异:
| 分子式 | 结构简式 | 熔点 | 沸点 | 水溶性 | |
| 乙醇 | C2H6O | C2H5OH | -114.3℃ | 78.4 °C | 互溶 |
| 二甲醚 | C2H6O | CH3OCH3 | -138.5℃ | -24.9℃ | 微溶 |
乙醇和二甲醚沸点及水溶性差异的主要原因是 。
(6)金属铜溶于在浓氨水与双氧水的混合溶液,生成深蓝色溶液。该深蓝色的浓溶液中加入乙醇可见到深蓝色晶体析出,请画出呈深蓝色的离子的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)下图是石墨的结构,其晶体中存在的作用力有 (填序号)
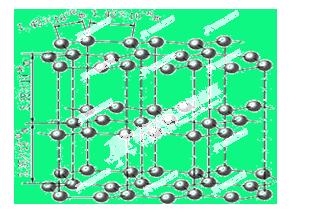
A.σ键 B.π键 C.氢键 D.配位键 E.分子间作用力 F.金属键 G.离子键
(2)下面关于晶体的说法不正确的是___________
A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小:NaF> NaCl> NaBr>NaI
(3)CaF2结构如图Ⅰ所示,Cu形成晶体的结构如Ⅲ所示,Ⅱ为H3BO3晶体结构图(层状结构,层内的H3BO3分子通过氢键结合)
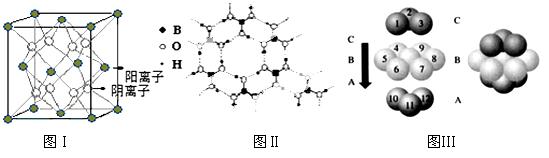
①图I所示的晶体中与Ca2+离子最近且等距离的Ca2+离子数为 ,
图III中未标号的Cu原子形成晶体后周围最紧邻的Cu原子数为 ;
② H3BO3晶体中B原子杂化方式______ ; CNO-的形状为____________;
③三种晶体中熔点高低的顺序为 (填空化学式),
H3BO3晶体受热熔化时,克服的微粒之间的相互作用为
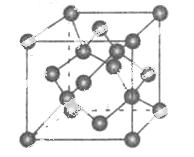
(4)碳的某种单质的晶胞如右图所示,一个晶胞中有_____个碳原子;若该晶体的密度为ρ g/cm3,阿伏加德罗常数的值为NA,则晶体中最近的两个碳原子之间的距离为_ ____cm(用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
2009年哥本哈根气候大会,是被称作“人类拯救地球的最后一次机会”的联合国气候变化大会。下列措施有利于节能减排、改善环境质量的是 ( )
①回收再利用废弃的塑料、金属、纸制品及玻璃等资源
②发展低碳经济、循环经济,开发推广太阳能、水能、风能等能源,减少煤、石油等化石燃料的使用 ③使用填埋法处理未经分类的生活垃圾 ④推广使用燃煤脱硫技术,防治SO2污染 ⑤研制开发新型燃料电池汽车,减少机动车尾气污染
A.①②④⑤ B.①②⑤
C.①②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+6HCl(浓)=
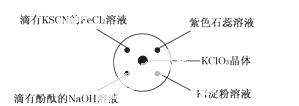
 ==KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( )
==KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红色 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
| C | 石蕊溶液先变为红色后褪色 | Cl2具有漂白性 |
| D | 淀粉KI溶液中变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,这是因为__________________________,反应的离子方程式是______________.
(2)在碘和淀粉形成的蓝色溶液中 通入SO2气体,发现蓝色逐渐消失,这是因为_______________,反应的离子方程式是___________________________________.
通入SO2气体,发现蓝色逐渐消失,这是因为_______________,反应的离子方程式是___________________________________.
(3)对比(1)和(2)实验所得的结果,将Cl-、I -、SO2按还原性由强到弱顺序排列为______________.
-、SO2按还原性由强到弱顺序排列为______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质具有以下性质:①是电解质 ②溶于水有化学键被破坏 ③熔化时没有化学键被破坏,则该物质固态时属于( )
A.原子晶体 B.离子晶体
C.分子晶体 D.何种晶体无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)检验某溶液中是否含SO 、CO
、CO 的正确操作顺序是:取少量未知溶液,先加入________,产生的气体可通过________,如出现________现象,证明原溶液含有________,接下的操作及现象是____________________________________________
的正确操作顺序是:取少量未知溶液,先加入________,产生的气体可通过________,如出现________现象,证明原溶液含有________,接下的操作及现象是____________________________________________
______________________________________________________。
(Ⅱ)现有A、B两种有机物的液体混合物,如果A、B互溶,且相互不发生化学反应。在常压下,A的沸点为35 ℃,B的沸点为200 ℃。回答下列问题:
(1)分离上述A、B的混合物,常用的方法是________,需要的玻璃仪器有酒精灯、温度计、牛角管、蒸馏烧瓶,还有________和________。
(2)应用上述分离操作,首先得到的物质是________。
(3)蒸馏烧瓶内碎瓷片的作用是________________。
(Ⅲ)下图是硫酸试剂瓶标签上的内容:

(1)该硫酸的物质的量浓度是________mol·L-1。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要240 mL 4.6 mol·L-1的稀硫酸,则需要取________mL的该硫酸。将上述硫酸进行稀释的实验操作为
___________________________________________________________________________________________________________________。
(3)用上述硫酸配制240 mL 4.6 mol·L-1的稀硫酸,实验仪器有:
①50 mL量筒 ②100 mL量筒 ③托盘天平 ④玻璃棒 ⑤250 mL容量瓶 ⑥胶头滴管 ⑦烧杯 ⑧锥形瓶
实验时使用选用仪器的先后顺序为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com