ClO
2�ڳ�������һ�ֻ���ɫ�д̼�����ζ�����壬���۵�Ϊ-59�棬�е�Ϊ11.0�棬������ˮ����ҵ�����Գ�ʪ��KClO
3�Ͳ��ᣨH
2C
2O
4����60��ʱ��Ӧ�Ƶã�ijѧ������ͼ1��ʾװ��ģ�ҵ��ȡ���ռ�ClO
2��

��1��Aװ�õ綯�������������
��Aװ�ñ��������¶ȿ���װ�ã����ƾ����⣬����Ҫ�IJ����������ձ���
��
��2��Bװ�ñ�����ڱ�ˮԡ�У���ԭ����
��
��3����Ӧ����װ��C�пɵ�NaClO
2��Һ����֪��1��NaClO
2������Һ���¶ȵ���38��ʱ����������NaClO
2?3H
2O�����¶ȸ���38��ʱ����������NaClO
2���¶ȸ���60��ʱNaClO
2�ֽ�����NaClO
3��NaCl����2��NaClO
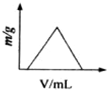
2���ܽ��������ͼ2��ʾ���벹���NaClO
2��Һ���Ƶ�NaClO
2����IJ������裺
�ټ�ѹ��55�������ᾧ����
����
����
���õ���Ʒ��
��4��ClO
2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO
2��Һ��Ϊ�ⶨ������Һ��ClO
2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO
2��Һ10.00mL��ϡ�ͳ�100.00mL��������ȡV
1 mL�������뵽��ƿ�У�
����2����ϡ�������������pH��2.0������������KI���壬����Ƭ�̣�
����3������ָʾ������c mol?L
-1 Na
2S
2O
3��Һ�ζ����յ㣬����Na
2S
2O
3��ҺV
2 mL����֪2Na
2S
2O
3+I
2�TNa
2S
4O
6+2NaI����
������100mL c mol?L
-1 Na
2S
2O
3����Һʱ���õ��IJ����������ձ�����Ͳ����������У�
��
�ڵζ������н�������ƽ�вⶨ��ԭ����
��
��ԭClO
2��Һ��Ũ��Ϊ
g?L
-1���ú���ĸ����ʽ��ʾ����
�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���
�����ƫ�ߡ�����ƫ�͡����䡱��

 CO�����ںϳɼ״�����ѹǿΪ0.1MPa�����£������ΪbL���ܱ������г���a mol CO��2a mol H2���ڴ��������ºϳɼ״���CO��g��+2H2��g��?CH3OH��g��ƽ��ʱCO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��
CO�����ںϳɼ״�����ѹǿΪ0.1MPa�����£������ΪbL���ܱ������г���a mol CO��2a mol H2���ڴ��������ºϳɼ״���CO��g��+2H2��g��?CH3OH��g��ƽ��ʱCO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�