

分析 B为黄绿色气体,应为Cl2,F为淡黄色化合物,应为Na2O2,由转化关系可知G为NaOH,H为红褐色沉淀,应为Fe(OH)3,则E为FeCl3,A为Fe,C为无色气体,应为O2,则D为Na,结合对应物质的性质以及题目要求解答该题.
解答 解:B为黄绿色气体,应为Cl2,F为淡黄色化合物,应为Na2O2,由转化关系可知G为NaOH,H为红褐色沉淀,应为Fe(OH)3,则E为FeCl3,A为Fe,C为无色气体,应为O2,则D为Na,
(1)由以上分析可知C为O2,故答案为:O2;
(2)F→G的反应为过氧化钠和水,生成氢氧化钠和氧气,方程式为2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(3)①由信息可知,发生2Fe3++SO2+H2O═2Fe2++SO42-+H+,则浅绿色溶液中一定存在的离子有H+、Cl-和Fe2+、SO42-,故答案为:Fe2+、SO42-;
②如果存在亚硫酸,亚硫酸分解生成二氧化硫和水,二氧化硫具有漂白性,能使品红溶液褪色,亚硫酸和稀硫酸、KSCN溶液不反应,和NaOH反应无明显现象,
故答案为:D;
(4)Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,
ClO-与ClO3-的物质的量浓度之比为5:1,
则可设ClO-为5mol,ClO3-为1mol,被氧化的Cl共为6mol,
失去电子的总物质的量为5mol×(1-0)+1mol×(5-0)=10mol,
氧化还原反应中氧化剂和还原剂之间得失电子数目相等,
Cl2生成NaCl是被还原的过程,化合价由0价降低为-1价,
则得到电子的物质的量也应为10mol,
则被还原的Cl的物质的量为10mol,
所以被还原的氯元素和被氧化的氯元素的物质的量之比为10mol:6mol=5:3,
故答案为:5:3;
(5)钠性质活泼,易与水、氧气反应,但密度比煤油大,可与煤油反应,故答案为:保存在煤油中;
(6)双氧水具有氧化性,在酸性环境下能将金属铜氧化,方程式为:Cu+H2O2+2HCl=CuCl2+2H2O,故答案为:Cu+H2O2+2HCl=CuCl2+2H2O.
点评 本题考查无机物推断,为高频考点,物质的颜色是推断突破口,结合中学常见物质及转化关系进行推断,需要学生具备扎实的基础与逻辑推理能力,难度中等


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 当pH=7时,若V1=V2,则一定是c2>c1 | |
| B. | 在任何情况下都满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 若pH>7,则一定是c1V1>c2V2 | |
| D. | 若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 1mol/L的稀硝酸中,氧原子数为3NA | |
| B. | 常温常压下的67.2L氯气与54g铝充分反应,转移电子数为6NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电数为0.2NA | |
| D. | 标准状况下,80gSO3,中含3NA心个氧原子,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
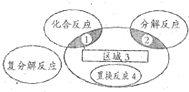
| A. | Br2+SO2+2H2O═H2SO4+2HBr | B. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | 4NH3+5O2═4NO+6H2O | D. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe与足量的Cl2反应转移的电子数为2NA | |
| B. | 标准状况下,22.4L水中含有的水分子数为NA | |
| C. | 常温、常压下,22gCO2中含有的氧原子数为NA | |
| D. | 0.11mol/LCaCl2溶液中含氧离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沙子硬度大,来源丰富,性质稳定,可用作混凝土中的填充材料 | |
| B. | 可用过量氨水除去MgCl2溶液中的AlCl3 | |
| C. | 工业上可用硫酸制化肥、农药、染料等 | |
| D. | 在煤中加入一些生石灰可以减少燃煤产生的二氧化硫的排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com