
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
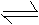 2N2O5(g) 4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
2N2O5(g) 4NO2(g)+O2(g) ΔH>0 ;T1温度下的部分实验数据为:
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是( )
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
D.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
【知识点】化学平衡常数计算、外界条件的影响
 【答案解析】D 解析:A、500 s内N2O5分解速率=(5.00-3.52)mol/L÷500s=2.96×10-3 mol·(L·s)-1,故A正确;
【答案解析】D 解析:A、500 s内N2O5分解速率=(5.00-3.52)mol/L÷500s=2.96×10-3 mol·(L·s)-1,故A正确;
B、T1温度下:2N2O5(g) 4NO2(g)+O2(g),
始态浓度: 5.00mol/L 0 0
变化浓度:2.50mol/L 5.00mol/L 1.25mol/L
平衡浓度:2.50mol/L 5.00mol/L 1.25mol/L
K=C(O2)·C4(NO2)/C2(N2O5)=125,1000 s时转化率=2.50÷5.00=50%;故B正确;
C、平衡常数只受温度影响,T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,反应吸热反应,则T1>T3,,故C正确;
D、该反应正反应是吸热反应,升高温度,反应速率加快,平衡向正反应移动,平衡时时N2O5(g)浓度应降低,其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,浓度大于2.5mol/L,故不可能为升高温度,应为降低温度,故T1>T2,所以D错误;
故答案选D
【思路点拨】本题考查化学平衡状态判断、化学平衡有关计算、化学平衡影响因素、平衡常数等,难度中等。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y 2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于:
2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于:
A、33% B、40% C、50% D、65%
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
A.使酚酞试液变红色的溶液:Na+、Ba2+、I-、Cl-
B.使甲基橙变红色的溶液:Ca2+、K+、HCO3-、Cl-
C.含有0.1 mol·L-1 Fe(NO3)2的溶液:H+、Mg2+、SCN-、Cl-
D.由水电离产生的c(H+)=10-13mol·L-1的溶液:NH4+、SO42-、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
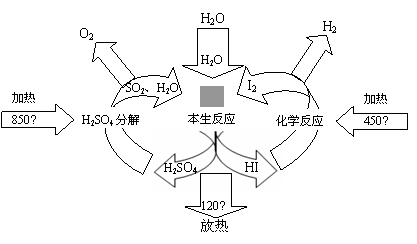 氢能是一种绿色能源,一种目前成熟的方法是利用碘硫热化学循环制备氢气,其原理示意图如下。
氢能是一种绿色能源,一种目前成熟的方法是利用碘硫热化学循环制备氢气,其原理示意图如下。
(1)已知:SO3(g)  SO2(g)+1/2O2(g) △H1 =-98.3kJ·mol-1
SO2(g)+1/2O2(g) △H1 =-98.3kJ·mol-1
H2SO4(l)  SO3(g) + H2O(l) △H2 =-130.4 kJ·mol-1
SO3(g) + H2O(l) △H2 =-130.4 kJ·mol-1
2H2SO4(l)  2SO2(g)+ O2(g)+ 2H2O(l) △H3
2SO2(g)+ O2(g)+ 2H2O(l) △H3
则△H3= kJ·mol-1 。
(2)上述热化学循环制氢要消耗大量的能量,从能源角度考虑,可采用的解决方案是
。
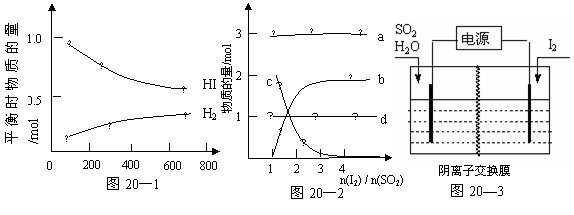
(3)碘化氢热分解反应为:2HI(g) H2(g) + I2(g),分解曲线如图20—1,分解反应平衡常数表达式为:K= ;升高温度时平衡常数K (选填:“增大”或“减小”)。
H2(g) + I2(g),分解曲线如图20—1,分解反应平衡常数表达式为:K= ;升高温度时平衡常数K (选填:“增大”或“减小”)。
(4)本生(Bunsen)反应中SO2和I2及H2O发生的反应为:SO2+I2+2H2O=3H++HSO4-+2I-,
I-+I2 I3-。
I3-。
①当起始时,SO2为1mol,水为16mol,溶液中各离子变化关系如图20—2,图中b变化表示的离子是 ;在水相中进行的本生反应必须使水和碘显著过量,但易
引起副反应将反应器堵塞等。写出浓硫酸与HI发生反应生成硫和碘的化学方程式
。
②野村(Nonura)等人提出利用电解的方法进行本生反应,反应原理如图20—3所示,则阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理研究元素及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+ O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如右图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如右图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

①2SO2(g) + O2(g) 2SO3(g)的△H____0(填“>”、“<”)。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”“向右”或“不移动”) 。
2SO3(g)的△H____0(填“>”、“<”)。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”“向右”或“不移动”) 。
②若温度为T1时,反应进行到状态D时,V正_______V逆(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产中有重要作用。
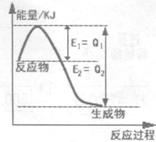
① 右图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式:(△H用含字母Q1、Q2的代数式表示) 。
②在AlCl3溶液中滴加氨水,反应的离子方程式为: 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25℃下,向0.1mol•L-1的NaCl溶液中逐滴加入适量的0.1mol•L-1硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1mol•L-1的NaI溶液,看到的现象是 全品教学网, 用后离不了!,产生该现象的原因是(用离子方程式表示): 。
全品教学网, 用后离不了!(已知25℃时Ksp[AgCl] =1.0×10-10 mol2•L-2,Ksp[AgI] =1.5×10-16mol2•L-2 )
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为8.96 L(0 ℃,1.01×105 Pa)时立即停止,则这一过程中,溶液中离子的物质的量与通入CO2气体的体积关系图像正确的是(气体的溶解和离子的水解忽略不计)
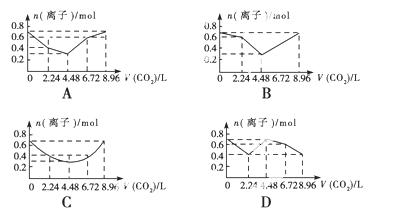
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究性学习小组利用下图中所列装置设计实验,证明浓硫酸和木炭粉在加热条件下反应有SO2和CO2生成。
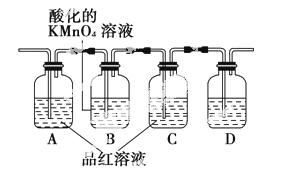
(1)实验时可观察到装置中A瓶溶液褪色,C瓶溶液不褪色。
A瓶溶液的作用是___________________________________,
B瓶溶液的作用是___________________________________,
C瓶溶液的作用是___________________________________。
(2)装置D中所盛溶液是________,可验证的产物是______。
(3)若想同时验证另一种产物的存在,需使用的药品为________,该装置在整套装置中的位置是________,理由是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是
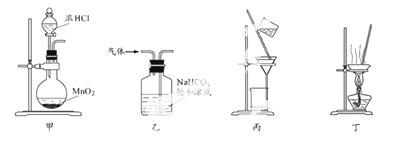
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于苯与乙烯的说法中正确的是( )
A.都能与酸性KMnO4溶液反应
B.等物质的量燃烧时苯消耗氧气多
C.都能与溴水发生加成反应
D.苯分子内所有原子共平面,分子内一个氢原子被甲基取代后,所有原子共面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com