
【题目】根据元素周期表和元素周期律分析下面的推断,其中不正确的是
A. Na的原子失去电子能力比Mg强
B. HBr比HCl稳定
C. Ca(OH)2 的碱性比 Mg(OH)2 的碱性强
D. H2SO4 比H3PO4 酸性强
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则 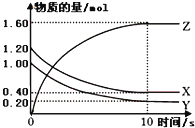
(1)①反应的化学方程式为; ②0~10s内,用Z表示的化学反应速率;
③X的转化率为;
(2)已知I2(g)为紫红色,在恒容容器中,可逆反应H2(g)+I2(g)2HI(g)达到平衡的标志是( )
A.混合气体密度恒定不变
B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等
D.混合气体的压强不再改变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“无论从经济的发展还是人类的进步而言,合成氨的发明都是本世纪科学领域中最辉煌的成就之一.”图1是与NH3相关的工业过程示意图. 
已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890kJmol﹣1
2CO(g)+O2(g)═2CO2(g)△H=﹣566.0kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H=﹣571.6kJmol﹣1
(1)请写出CH4(g)与O2(g)反应生成CO(g)和H2(g)的热化学反应方程式 .
(2)在生产过程中,会涉及H2和CO2的分离.你认为可取的方法是(填序号).
a.在加压条件下用水吸收CO2 b.用NaOH溶液吸收CO2 c.加压,使CO2液化
(3)合成尿素的反应是分作两步进行的:
①CO2(g)+2NH3(g)═H2NCOONH4(aq) (氨基甲酸铵)△H=﹣159.47kJmol﹣1
②H2NCOONH4(aq)═CO(NH2)2(aq)+H2O(l)△H=﹢28.49kJmol﹣1
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如图2所示.生产过程中n(NH3):n(CO2)的最佳配比为 , 而实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为、 . 在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 .
(4)将氨分为两部分,一部分经逐级氧化吸收转化为硝酸,另一部分又与HNO3反应生成NH4NO3 . 若HNO3与NH3的反应是完全的,有标准状况下50LNH3经上述反应过程生成84g NH4NO3 . 则NH3逐级转化为HNO3的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O的说法正确的是( )
A. Cu是氧化剂
B. 该反应电子转移总数为4e—
C. 硝酸在反应中只体现氧化性
D. NO是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是( )
A.反应速率:两者相同
B.消耗HNO3的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的反应产物质量最大
D.第二块钠的反应产物在空气中更稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列由于物质的漂白性而导致溶液褪色的是( )
①将过氧化钠投入水中,然后加入几滴酚酞溶液,溶液先变红后褪色
②将活性炭放入红墨水中,溶液褪色
③向品红溶液中滴加氯水,红色褪去
④向酸性高锰酸钾溶液中通入二氧化硫气体,溶液紫色褪去
A.①③
B.①②③
C.①②③④
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e-稳定结构的物质可能是(写分子式)。元素⑨和⑩形成的化合物的化学式为;元素①的原子价电子排布式是。
(3)①、⑥、⑦、⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是(填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是(填名称),可以验证你的结论的是下列中的(填序号)。
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表③和⑨两元素)
F.两单质在自然界中的存在形式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,同 体积的NH3和H2S气体的质量之比为______________;同质量的NH3和H2S气体的体积之比为________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com