
【题目】现有下列可逆反应:A(g)+B(g) ![]() xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
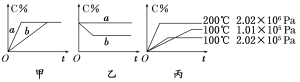
请根据图像回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性(与反应体系中任一物质均不反应)气体后的情况,则 曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填“吸”或“放”);
(4)化学计量数x的值 (填取值范围);判断的依据是 。
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是
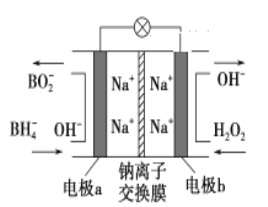
A. 电池工作时Na+从b极区移向a极区
B. a极上的电极反应式为:BH4-+8OH--8e-===BO2-+6H2O
C. 每消耗3 mol H2O2,转移3 mol e-
D. b极上的电极反应式为:H2O2+2e-+2H+===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂排放的SO2烟气对环境造成污染,某企业用下图流程综合处理,下列有关说法正确的是

A. 二氧化硫吸收塔中发生的反应为SO2+SO32—+H2O=2HSO3—
B. 氨气吸收塔中发生的反应为HSO3—+OH-=H2O+SO32—
C. 上述流程利用的是氧化还原反应原理
D. 上述流程可循环利用的物质有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是
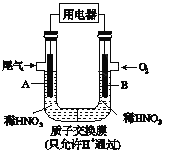
A. 电极A表面反应之一为NO2-e-+H2O= NO3_+2H+
B. 电极B附近的c(NO3_)增大
C. 电解质溶液中电流的方向由B到A,电子的流向与之相反
D. 该电池工作时,每转移4mol电子,消耗22.4L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量。
(1)配平以下离子方程式,并在□中填上合适的微粒:
________![]() ________
________![]() ________
________![]() ________
________![]() ________
________![]() ________________
________________
(2)测定血钙的含量:取2 mL血液用蒸馏水稀释后,向其中加入足量![]() 溶液,反应生成
溶液,反应生成![]() 沉淀,过滤并洗涤沉淀,将沉淀用稀硫酸溶解得到
沉淀,过滤并洗涤沉淀,将沉淀用稀硫酸溶解得到![]() 后,再与一定量的
后,再与一定量的![]() 溶液恰好完全反应。溶解沉淀时________(填“能”或“不能”)使用稀盐酸,原因是____________。
溶液恰好完全反应。溶解沉淀时________(填“能”或“不能”)使用稀盐酸,原因是____________。
(3)若消耗了![]() 的
的![]() 溶液40.00 mL,则100 mL该血液中含钙________g。
溶液40.00 mL,则100 mL该血液中含钙________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为:Na2Cr2O7·2H2O),其主要工艺流程如下:
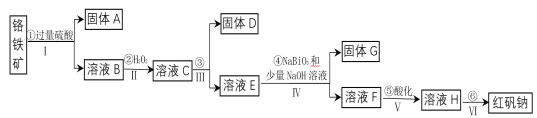
查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42—,自身被还原为Bi(OH)3固体。
ii.
物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 | Bi(OH)3 |
开始沉淀的PH | 2.7 | 3.4 | 4.6 | 7.5 | 0.7 |
完全沉淀的PH | 3.7 | 4.4 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)将铬铁矿矿石粉碎的目的是___________。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和___________(填仪器名称)。
(3)写出④反应的化学方程式________________。
(4)⑤中酸化是使CrO42—转化为Cr2O72—。写出该反应的离子方程式______。
(5)将溶液H经下列操作:蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
(6)取一定质量的固体D溶解于200mL的稀硫酸中,向所得溶液中加入5.0mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为_________,固体D中含Fe化合物的物质的量为___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①漂白粉、水玻璃、福尔马林都是混合物
②砹(At)是第ⅦA族,AgAt 易溶于水
③用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
④Cs2CO3加热时不能分解为CO2和Cs2O
⑤纳米铁粉可以除被污染水体中的重金属离子
⑥根据反应SiO2+CaCO3![]() CaSiO3+CO2↑可推知硅酸酸性比碳酸强
CaSiO3+CO2↑可推知硅酸酸性比碳酸强
A. ①③④⑤ B. ①④⑤ C. ③④⑤⑦ D. ①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是
A. 2Na+2H2O===2NaOH+H2↑
B. Cl2+H2O===HCl+HClO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. Ca(ClO)2+2HCl===CaCl2+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了利用氯酸钾分解制O2测定气体摩尔体积的探究实验。实验步骤如下:

①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
②连接好实验装置,
③加热,开始反应,直到不再有气体产生为止
④测量排入量筒中水的体积为279.7 mL
⑤准确称量试管和残留物的质量为15.55 g
根据上述实验过程,回答下列问题:
(1)请补充②中的实验步骤___________________。
(2)以下是测量收集到气体体积必须包括的几个步骤:
a.调整量筒的高度使广口瓶和量筒内的液面高度相同;b.使试管和广口瓶内气体都冷却至室温;c.读取量筒内液体的体积。这三步操作的正确顺序是________(请填写步骤序号)。进行实验操作c时,若仰视读数,则读取氧气的体积______(填“偏大”、“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是__________mol;实验测得该条件下的气体摩尔体积是____(保留小数点后两位)。
(4)若欲检验试管中产物所含的阴离子,方案为:将固体冷却后溶于水,过滤,_________________________________(填写具体实验方案)。若想检验产物中所含的阳离子方法为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com