
铅蓄电池是典型的可充电型电池,它的正负极极板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO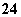
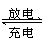
 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是____________________________________________;
电解液中H2SO4浓度将变____;电流方向从____极流向____极。当外电路通过1 mol电子时,理论上负极板的质量增加________g。
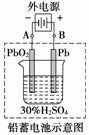
(2)在完全放电耗尽PbO2和Pb时,若按如图连接,电解一段时间后,则在A电极上生成______、B电极上生成________,此时铅蓄电池的正负极的极性将________。
答案 (1)PbO2+2e-+4H++SO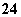 —→PbSO4+2H2O 小 正 负 48 (2)Pb PbO2 对换
—→PbSO4+2H2O 小 正 负 48 (2)Pb PbO2 对换
解析 解答本题要注意以下两点:
(1)原电池正极、电解池阴极发生还原反应,原电池负极、电解池阳极发生氧化反应。
(2)铅蓄电池完全放电后,电极材料为PbSO4。
原电池中正极上得电子、负极上失电子。根据电池总反应式,正极反应为:PbO2+2e-+4H++SO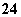 —→PbSO4+2H2O。
—→PbSO4+2H2O。
负极反应为:
Pb+SO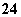 —→PbSO4+2e- 质量增加
—→PbSO4+2e- 质量增加
2 mol 96 g
1 mol Δm
求得Δm=48 g
电解池里与电源正极相连的电极(阳极)上失电子、与电源负极相连的电极(阴极)上得电子。则阳极反应式为PbSO4+2H2O—→PbO2+4H++SO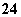 +2e-;阴极反应式为PbSO4+2e-—→Pb+SO
+2e-;阴极反应式为PbSO4+2e-—→Pb+SO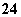 。根据图示,电解一段时间后,原PbO2极(阴极)变成Pb, 原Pb极(阳极)变成PbO2,即正负极对换。
。根据图示,电解一段时间后,原PbO2极(阴极)变成Pb, 原Pb极(阳极)变成PbO2,即正负极对换。


科目:高中化学 来源: 题型:
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( )
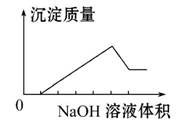
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
增塑剂(又叫塑化剂)是一种增加塑料柔韧性、弹性等的添加剂,不能用于食品、酒类等行业。DBP(邻苯二甲酸二丁酯)是增塑剂的一种,可由下列路线合成:

已知:

②R1CHO+R2CH2CHO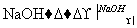
 +H2O (—R1、—R2表示氢原子或烃基)
+H2O (—R1、—R2表示氢原子或烃基)
请回答下列问题:
(1)A→B的反应类型为____________,D→E的反应类型为____________。
(2)DBP的分子式为__________,D的结构简式是__________。
(3)写出B和E以物质的量之比1∶2反应生成DBP的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧燃料电池用于航天飞机,电极反应产生的水经冷凝后可作为航天员的饮用水,其电极反应式如下:

负极:2H2+4OH-—→4H2O+4e-
正极:O2+2H2O+4e-—→4OH-
当得到1.8 L饮用水时,电池内转移的电子数约为( )
A.1.8 mol B.3.6 mol C.100 mol D.200 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
芳香族化合物A,分子式为C9H9OCl,且能发生银镜反应;D为含有八元环的芳香族化合物。A与其它物质之间的转化如下图所示:

(1)A的结构简式为 。
(2)A→E的反应条件为 ;C→D的反应类型为 。
(3)写出B→C第①步的反应方程式 。
(4)B的一种同系物F(分子式为C8H8O2)有多种同分异构体,则含有 的芳香族化合物的同分异构体有 种,写出其中核磁共振氢谱有4个峰的一种结构简式 。
的芳香族化合物的同分异构体有 种,写出其中核磁共振氢谱有4个峰的一种结构简式 。
(5)已知: 由甲苯及其它必要物质经如下步骤也可合成B:
由甲苯及其它必要物质经如下步骤也可合成B:

反应I的试剂及条件为 :反应IV所用物质的名称为 ;
反应III的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示水槽中试管内有一枚铁钉,放置数天观察:
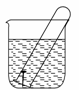
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于________腐蚀。
(2)若试管内液面上升,则原溶液呈________________性,发生________腐蚀,电极反应式:负极: _____________________________________________________________,
正极: _______________________________________________________________。
(3)若试管内液面下降,则原溶液呈______性,发生________腐蚀。电极反应式:负极
________________________________________________________________________,
正极: ______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上消除氮氧化物的污染可用如下反应:
CH4(g)+2NO2(g)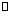 N2(g)+CO2(g)+2H2O(g)
N2(g)+CO2(g)+2H2O(g) 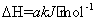
在温度T1和T2时,分别将0.50molCH4和1.2molNO2充入体积为1L的恒容密闭容器中,测得n(N2)随时间变化的数据如下表:
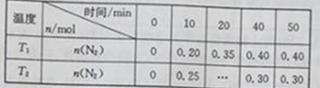
下列说法不正确的是
A. 10min内,T1时的v(N2)比T2时的小
B. T1<T2
C. a<0
D. T2时,若向平衡后的容器中再充入1.2molCH4,重新达到平衡时n(N2)=0.40mol
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中提取镁的工艺流程可表示如下:
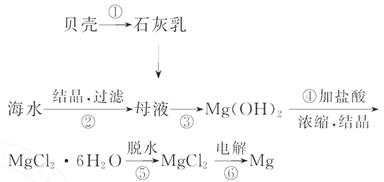
下列说法不正确的是( )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.步骤⑤可将晶体置于HCl气体氛围中脱水
D.上述工艺流程中涉及化合、分解和复分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com