
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究:
Ⅰ.在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
Ⅱ.过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
Ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生,
经检测,上述实验中产生的无色气体均为CO
2.
(1)按要求写出下列反应的离子方程式:
①实验室用二氧化锰和浓盐酸制取氯气
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
.
②氯气与水
Cl2+H2O?H++Cl-+HClO
Cl2+H2O?H++Cl-+HClO
.
(2)依据上述定性实验:
①反应后所得的溶液比氯水漂白性增强的原因是
碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强
碳酸钙消耗了氯水中的H+,使Cl2+H2O?H++Cl-+HClO平衡正向移动,HClO浓度大,漂白效果增强
.
②由此可推知,Ⅱ的滤液中的溶质除CaCl
2、HClO外,还含有
Ca(HCO3)2
Ca(HCO3)2
.

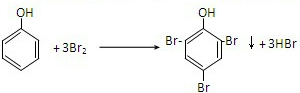 ,故答案为:
,故答案为: ,
,



 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究: