
下列关于电解质溶液的判断正确的是( )
A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO3—、SO32-、K+可以大量共存
C.由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液中存在BOH===B++OH-
D.由0.1 mol·L-1一元酸HA溶液的pH=3,可推知NaA溶液中存在A - +H2O HA+OH-
HA+OH-
科目:高中化学 来源: 题型:
单质A、B、C和化合物D、E、F,在一定条件下有如下图的转化关系:(有部分反应物或者生成物未标出)
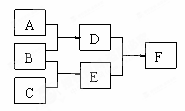
请回答下列问题:
(1)若A是空气中含量最多的气体,B在C中燃烧火焰呈苍白色。A与B反应生成D的化学方程式是__________________。D与E反应的现象是___________。D在催化剂作用下被氧气氧化是工业制备硝酸的主要反应之一,该反应的化学方程式是_____________。
(2)若A是金属单质,D是淡黄色固体,E在空气中含量增加会导致温室效应。则D的用途之一是__________,D与E反应生成F的化学方程式是__________________________。可以通过______________实验来检验D和F中所含的金属元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2 丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是____ ________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):

(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明_ _______
② 称取Mg(NO3)2固体3 . 79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是________;关闭K,用酒精灯加热时,正确操作是先________然后固定在管中固体部位下加热。
③ 观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④ 待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g
⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
① 根据实验现象和剩余固体的质量经分析可初步确认猜想_______是正确的。
② 根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应: _________________ ____(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是_____________________。
③ 小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分子中既有σ键又有π键的是( )
①Cl2 ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥CO2
A.①②③ B.③④⑤⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关系的表述中,正确的是( )
A.0.1 mol·L-1 NaHSO4溶液中:c(Na+)+ c(H+) = c(SO42 -)+c(OH-)
B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1∶1
C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等
D.0.1 mol·L-1 NaHCO3溶液中:c(Na+)>c(HCO3- )>c(CO32-)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下进行反应A(g) B(g)+xC(g),反应开始时容器中只含有A,其相对分子质量为32,平衡时混合气体的平均相对分子质量为20,此时A的转化率为30%,则x的值为( )
B(g)+xC(g),反应开始时容器中只含有A,其相对分子质量为32,平衡时混合气体的平均相对分子质量为20,此时A的转化率为30%,则x的值为( )
A、1 B、2 C、3 D、4
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z四种元素原子序数依次减小。已知W的原子序数为29;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能数据如下表;Z原子价电子排布式为nsnnpn。请回答下列问题:
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1 823 | 2 751 | 11 584 | 14 837 |
(1)W基态原子的电子排布式为______________。
(2)电负性:X________Y(填“>”、“=”或“<”)。
(3)R是与X同主族的短周期元素。R的氢化物沸点比X的氢化物高,原因是______。
(4)Z2X4中,Z原子采用________杂化,每个分子中含有________个σ键,________个π键。
(5)已知W2+能与氨分子形成配离子[W(NH3)4]2+,该配离子中存在的化学键有________。(填标号)
A.金属键 B.离子键 C.共价键 D.配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
把少量的溴水注入KI溶液中,经充分反应后,加入CCL4用力振荡,静置后可观察到
A.液体分成两层,下层呈紫色 B.液体分成两层,上层呈紫色
C.混合液不分层,且无色透明 D.混合液不分层,且呈褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中的每一方框内表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且A与C物质的量之比为1:1。B为常见液体。
试回答下列问题:
(1)X是__________________; F是___________________。
 (2)A D反应的化学方程式并标出电子转移的方向和数目_______________________________。
(2)A D反应的化学方程式并标出电子转移的方向和数目_______________________________。
(3)G与Cu的反应中,G表现_______________________性质。
(4)X与过量NaOH溶液反应的离子方程式: 。
(5)以C、B、D为原料可生产G,若使a mol C 完全转化为G,理论上至少需要D ____________mol 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com