
| A、①② | B、②⑤ | C、⑤ | D、④ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
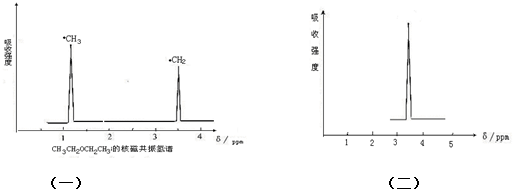
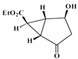
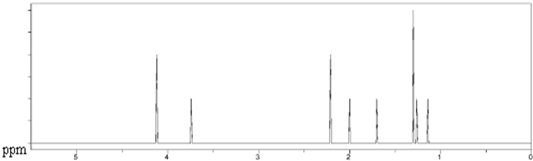
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇(乙酸) NaOH溶液 分液 |
| B、乙烯(SO2) KMnO4溶液 洗气 |
| C、乙烷(乙烯) H2(催化剂) 催化加氢 |
| D、乙醇(水) CaO 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不用其它试剂便无法区别NaCl、Na2CO3、NaHSO4、AlCl3四种溶液 |
| B、纤维素水解与淀粉水解得到的最终产物不同 |
| C、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量相等 |
| D、用渗析的方法精制氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a可能为6 |
| B、a可能为5 |
| C、a可能为4 |
| D、a可能为3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
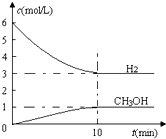 T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )
T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )| A、0~10 min 内υ(H2)=0.3 mol/(L?min) | ||
B、T℃时,平衡常数K=
| ||
| C、T℃时,若上述反应中有64 g CH3OH生成,则同时放出98.0 kJ的热量 | ||
| D、达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石蕊可作为判断终点的指示剂 |
| B、滴定时,控制滴加速率:先快后慢 |
| C、标准溶液的浓度越大,滴定误差越小 |
| D、滴定时,眼睛注视滴定管内液面的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NO3-、K+、SO42ˉ |
| B、Ca2+、H+、CO32ˉ、Cl- |
| C、OHˉ、SO42ˉ、NH4+、Al3+ |
| D、Fe3+、Mg2+、NO3ˉ、Clˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测定中和热时,大小两烧杯间填满碎纸的作用只是固定小烧 杯 |
| B、若用50mL 0.55mo1?L-1的氢氧化钠溶液,分别与50mL 0.50mo1?L-1的盐酸和50mL 0.25mo1?L-1的硫酸充分反应,两反应测定的中和热不相等 |
| C、实验时需要记录初始温度T1和最高温度T2 |
| D、酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com