
| A����0.1mol?L-1 CH3COONa��Һ�У�c��OH-��=c��CH3COOH��+c��H+�� |
| B��0.1mol?L-1��KAl��SO4��2��Һ�У�c��SO42-����c��Al3+����c��OH-����c��H+�� |
| C��pH��ȵ�NaOH��CH3COONa��NaHCO3������Һ�����У�c��NaOH����c��CH3COONa����c��NaHCO3�� |
| D��������������ʵ���Ũ�ȵ�NaX������HX��Ϻ����Һ������Һ�����ԣ�����c��Na+����c��HX����c��X-����c��H+����c��OH-�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����������·�ߺϳɣ�
����������·�ߺϳɣ�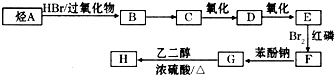
| HBr/�������� |
| Br2/���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���ӳɷ�Ӧ | B��ȡ����Ӧ |
| C��ˮ�ⷴӦ | D����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ơ�� | B���� | C�����Ѿ� | D���ƾ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��I2��FeCl3��Cl2��Co2O3 |
| B��Co2O3��Cl2��FeCl3��I2 |
| C��Cl2��Co2O3��I2��FeCl3 |
| D��Cl2��I2��Co2O3��FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
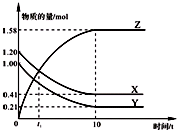 һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ���ǣ�������
һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ���ǣ�������| A����Ӧ��ʼ��10 s����Z��ʾ�ķ�Ӧ����Ϊ0.158 mol/��L?s�� |
| B����Ӧ��ʼ��10 sʱ��Y��ת����Ϊ79.0% |
| C��t1ʱ��Z��X��Ũ����ȣ��ﵽ�˻�ѧƽ��״̬ |
| D����Ӧ�Ļ�ѧ����ʽΪ��X��g��+Y��g��?Z��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol CH4��g����2mol O2��g���������ܺ�С��1mol CO2��g����2mol H2O��g���������ܺ� |
| B����״���£�44.8L NO��22.4L O2��Ϻ������з�������С��2NA |
| C��1mol Fe�������г��ȼ��ʧȥ3NA������ |
| D���ڱ�״���£�NA��CHCl3������ռ�����ԼΪ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ca��HCO3��2��Һ�м�������NaOH��Һ��Ca2++2HCO3-+2OH-�TCaCO3��+CO32-+H2O | ||||
| B����������������ϡ���3Fe2++4H++NO3-�T3Fe3++NO��+3H2O | ||||
| C������0.4mol FeBr2����Һ��ͨ��0.3mol Cl2��ַ�Ӧ��4Fe2++2Br-+3Cl2�T4Fe3++6Cl-+Br2 | ||||
D����ͭΪ�缫��ⱥ��ʳ��ˮ��2Cl-+2H2O
|
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com