
| A�� | Ӥ���õġ���ʪ�������������������ļ��ٱ�����Һ�����β�©������Ϊ�����������м�����������ˮ����Ե�� | |
| B�� | ������ά���������ӡ������������ά�����Ƴɣ����ϳ���ά��������Ȼ��ķ���ά���ϣ���ʯ�͡�ú��ͨ����ѧ�ϳɷ����õ� | |
| C�� | �μ�أ����϶�NaCl��Na2CO3����ͨ��ʩ������ʯ�ཱུ�������ļ��� | |
| D�� | ������ʳ��ƾ����˵��ۡ������ǡ��Ҵ��Ļ�ѧ�仯���� |
���� A������ʪ���м������ˮ�����л��
B������Ȼ��ά����ά����Ƥ��ֽ��������ɴ��Ϊԭ�����ڷ�˿����ɴ����ģ�����������ά��ʯ�ͻ���Ϊԭ������ģ����Ǻϳ���ά��
C��Na2CO3��CaSO4��Ӧ���������Ե�̼��ƣ�ͬʱ����ǿ��ǿ���������ƣ�
D�����ۡ������ǡ��Ҵ����ǻ�ѧ�仯��
��� �⣺A������ʪ���м������ˮ�����л�����������A����
B������Ȼ��ά����ά����Ƥ��ֽ��������ɴ��Ϊԭ�����ڷ�˿����ɴ����ģ�����������ά����ʯ�ͻ���Ϊԭ������ģ����Ǻϳ���ά����B��ȷ��
C��ʯ������Ҫ�ɷ���CaSO4��Na2CO3��CaSO4��Ӧ���������Ե�̼��ƣ�ͬʱ����ǿ��ǿ���������ƣ���������Ӻ������Ӳ�ˮ�⣬������Һ�����ԣ�����ʯ���ܽ�������ԣ���C��ȷ��
D������ʳ���ʱ�������ǻ�ø������ˮ��Ϊ�����ǣ�Ȼ���ڽ�ĸ������ת��Ϊ�ƾ������ǻ�ѧ�仯����D��ȷ����ѡA��
���� ������Ҫ����������Ļ�ѧ��ص�֪ʶ���������ʵijɷ֡��л��߷��Ӳ��ϡ���ʳ��Ƶ�֪ʶ�ǽ��Ĺؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢܢ� | B�� | �٢ڢۢܢ� | C�� | �ܢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ά�ء������ʶ����л��߷��ӻ����� | |
| B�� | �����ױ�����ú����Ҫ�ɷ� | |
| C�� | �����͡�ţ�Ͷ������� | |
| D�� | ������ţ�̿���Ϊ��ʳ�ؽ����εĽⶾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ס�ֲ��ո˵���ԭ�������Ҵ�������������ȼ�� | |
| B�� | �ö���Ĺǻ�Ƥ��ԭ��������ҩ�������̲�Ʒ | |
| C�� | �õ�����ԭ����ȡ����ø���������� | |
| D�� | ��ֲ���ͻ���֬����ԭ������������ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
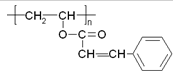 ��̽��Ǵ��ģ���ɵ�·ӡˢ��·�漼���еĹؼ����ijһ��̽�����Ҫ�ɷ���ͼ��ʾ�������й�˵����ȷ���ǣ�������
��̽��Ǵ��ģ���ɵ�·ӡˢ��·�漼���еĹؼ����ijһ��̽�����Ҫ�ɷ���ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | �ϳɴ˸߾���ĵ���Ļ�ѧʽΪC11H10O2 | |
| B�� | �����ʿ��ȶ������ڼ�����Һ�� | |
| C�� | 1mol������������3molH2�����ӳɷ�Ӧ | |
| D�� | �����ʿɾ������۷�Ӧ�Ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��c��NaOH����c��Na2CO3����c��CH3COONa�� | |
| B�� | pH=5�Ģ�NH4Cl��Һ��CH3COOH��Һ��������Һ����ˮ�������c��H+�����٣��ڣ��� | |
| C�� | �����pH=12��NaOH��Һ��pH=2��CH3COOH��Һ��ϣ���Ϻ���ҺpH��7 | |
| D�� | 0.1mol•L-1��CH3COOH��ҺpH=a��0.01mol•L-1��CH3COOH��ҺpH=b����b��a+1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ƶĵ���ʽ��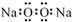 | |
| B�� | �����á���������ʹ�õ�������94��������144����ԭ�ӣ�${\;}_{94}^{144}$Pu | |
| C�� | CH4�����ģ�ͣ�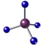 | |
| D�� | Na��ԭ�ӽṹʾ��ͼ��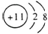 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��1���к���ɫ�����2���к���ɫ��dz | B�� | ��1���к���ɫ��dz����2���к���ɫ���� | ||
| C�� | ��ƿ��1���������ѹǿ���� | D�� | ��ƿ��2���������ѹǿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���л�ѧ�̲Ľ������ơ�þ�����������ȡ��������Ԫ�ؼ��仯�����֪ʶ����ѧϰ�о�������ѧ֪ʶ�����壮
���л�ѧ�̲Ľ������ơ�þ�����������ȡ��������Ԫ�ؼ��仯�����֪ʶ����ѧϰ�о�������ѧ֪ʶ�����壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com