
| A. | 醋酸可用于清除水垢 | B. | 蛋白质遇碘水显蓝色 | ||
| C. | 液化石油气的主要成份为CH4 | D. | 煤的液化属于物理变化 |
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:解答题
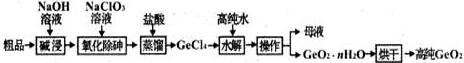
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
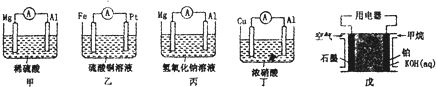
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中c(OH-)减小 | B. | pH的变化值小于2 | ||
| C. | 溶液中H+的数目增大 | D. | Kw的值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
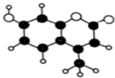 有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )| A. | 分子中含有3种官能团 | |
| B. | 1 mol该有机物与足量溴水反应最多消耗3molBr2 | |
| C. | 1 mol该有机物最多能与2 mol NaOH反应 | |
| D. | 该有机物若能使酸性KMnO4溶液褪色,则可证明其分子中存在碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
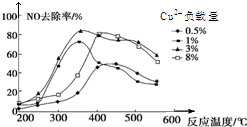 雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:
雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂在NaOH热溶液中完全水解后,加入热饱和食盐水可观察到液面上有固体析出 | |
| B. | 容量瓶、滴定管和分液漏斗均标有“O”刻度线,使用前均需要检漏 | |
| C. | 实验室用二氧化锰与浓盐酸制氯气时,先加热二氧化锰再滴加浓盐酸 | |
| D. | 为检验摩尔盐中的NH4+,可向试样加入少量的稀Na0H,再用pH试纸检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com