

���� ��1��ʹ�ô���ͨ���ı䷴Ӧ�����̣����ͷ�Ӧ�Ļ�ܣ������˻������Ŀ����ٷֺ������ӿ췴Ӧ���ʣ�
��2������ͼ1д����Ӧ���Ȼ�ѧ����ʽ�������Ȼ�ѧ����ʽ��������0.75mol/L��2L=1.5mol�Ҵ��ų���������
��3��������ʼ����ƽ��������ת���ʣ�
��4��2CH3OH+3O2?2CO2+4H2OΪ���ȷ�Ӧ�������¶�ƽ���������ƶ����ݴ��ж�K�仯��
���������ӵ��ƶ������ж�ȼ�ϵ�صĵ缫����������������Ӧ������������ԭ��Ӧ��
��� �⣺��1��ʹ�ô���ͨ���ı䷴Ӧ�����̣����ͷ�Ӧ�Ļ�ܣ������˻������Ŀ����ٷֺ������ӿ췴Ӧ���ʣ�
��ѡ��A��
��2������ͼ1д����Ӧ���Ȼ�ѧ����ʽ��CO��g��+2H2��g��?CH3OH��g����H=-91KJ/mol��
����ͼ2��֪��Ӧ�ﵽƽ��ʱ�����Ҵ�1.5mol����Ӧ��Ϊ��-91KJ/mol��1.5mol=-136.5KJ/mol���ų�����136.5KJ��
�ʴ�Ϊ��136.5��
��3����ͼ2��֪����Ӧ�м�С��CO��Ũ��Ϊ1mol/L-0.25mol/L=0.75mol/L��10minʱ�ﵽƽ�⣬
���ݷ���ʽ��
CO��g��+2H2��g��?CH3OH��g��
��ʼ 1mol/L 2mol/L 0
ת�� 0.75mol/L 1.5mol/L 0.75mol/L
ƽ�� 0.25mol/L 0.5mol/L 0.75mol/L
CO��ת����Ϊ$\frac{0.8mol/L}{1mol/L}$��100%=80%���ʴ�Ϊ��80%��
��4��2CH3OH+3O2?2CO2+4H2OΪ���ȷ�Ӧ�������¶�ƽ���������ƶ����÷�Ӧ��ƽ�ⳣ��K����С�������õ�ؽ���ѧ��ת��Ϊ���ܣ�
���������������֪b�缫Ϊ������a�缫Ϊ��������������������Ӧ���״���b��ʧȥ���ӷ���������Ӧ���ɶ�����̼�������ӣ��缫��ӦʽΪ��CH3OH+H2O-6e-=CO2��+6H+��
�ʴ�Ϊ�������ڣ�a��CH3OH+H2O-6e-=CO2��+6H+��
���� �����漰�绯ѧ���Ȼ�ѧ�Լ���ѧ��Ӧ���ʺ�ƽ����ۺ�֪ʶ�Ŀ��飬ע�⻯ѧƽ�ⳣ���ļ��㼰�����壬��Ŀ�Ѷ��еȣ�


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaH����ԭ | |
| B�� | NaH���������� | |
| C�� | H2O�Ȳ����������ֲ��ǻ�ԭ�� | |
| D�� | ������22.4 L��״���µ�H2������1 mol����ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
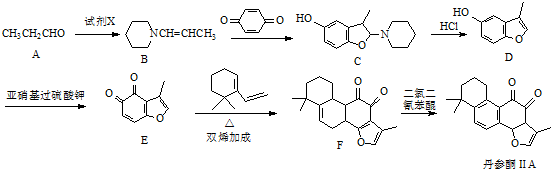
 ��
�� ��
�� �ĺϳ�·������ͼ�����Լ�����ѡ�����ϳ�·������ͼʾ�����£�CH3CHO$��_{��������}^{O_{2}}$CH3COOH$��_{ŨH_{2}SO_{4}����}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3��
�ĺϳ�·������ͼ�����Լ�����ѡ�����ϳ�·������ͼʾ�����£�CH3CHO$��_{��������}^{O_{2}}$CH3COOH$��_{ŨH_{2}SO_{4}����}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �¶�/�� | 1000 | 1100 |
| ƽ�ⳣ�� | 0.68 | 0.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������غ㶨�ɣ�������������һ�����ڷ�Ӧ�������� | |
| B�� | ���ȷ�Ӧ�ķ�Ӧ����һ���������ȷ�Ӧ�ķ�Ӧ���� | |
| C�� | ��ʾ�к��ȵ��Ȼ�ѧ����ʽ��NaOH+HCl�TNaCl+H2O��H=-57.3 kJ•mol-1 | |
| D�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��40gNaOH����1Lˮ���õ���Һ | |
| B�� | ���³�ѹ�£���22.4LHCl��������ˮ���1L������Һ | |
| C�� | ��23gNa����ˮ�����1L��Һ | |
| D�� | ��K+Ϊ1 mol•L-1��K2SO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com