
| A、煤 | B、海水 | C、石油 | D、天然气 |


科目:高中化学 来源: 题型:
A、CaCO3
| ||||
B、2Al+Fe2O3
| ||||
| C、2Na+2H2O=2NaOH+H2↑ | ||||
| D、H2SO4+2NaOH═Na2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO溶液的消毒原理是使蛋白质变性 |
| B、1molCl2与足量NaOH溶液反应转移1mol电子 |
| C、NaClO溶液的漂白原理与Na2O2、SO2相同 |
| D、“84”消毒液不能与“洁厕灵”(盐酸)共同使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
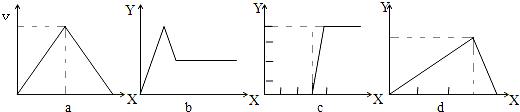
| A、①a | B、②b | C、③c | D、④d |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、观察容量瓶刻度线时仰视 |
| B、小烧杯,玻璃棒没有洗涤 |
| C、所用容量瓶中已有少量水 |
| D、观察容量瓶刻度线时俯视 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com