
【题目】某温度下,向10 mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,溶液中-lgc(Cu2+)与滴加的Na2S溶液体积(V)的关系如图所示(忽略体积变化)。下列判断正确的是
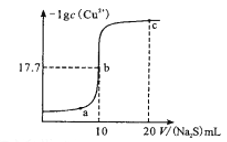
A. a、b、c三点中,b点水的电离程度最大
B. a点:2c(Cu2+)+c(H+)=c(Cl-)+c(OH-)
C. c点溶液:c(Cu2+)=3×10-34.4mol/L
D. c点溶液有:n(S2-)+n(HS-)+n(H2S)=n(Cl-)
【答案】C
【解析】A、Cu2+或S2-均会水解,水解促进水的电离,b点溶液时滴加Na2S溶液的体积是10mL,此时恰好生成CuS沉淀,b点溶液中水的电离程度最小,A错误;B、根据电荷守恒可知a点溶液中2c(Cu2+)+c(H+)=2(S2-)+c(Cl-)+c(OH-),B错误;C、b点时滴加Na2S溶液的体积是10mL,此时恰好生成CuS沉淀,CuS存在沉淀溶解平衡:CuS(s)Cu2+(aq)+S2-(aq),已知此时-lgc(Cu2+)=17.7,则平衡时c(Cu2+)=c(S2-)=10-17.7mol/L,因此硫化铜的溶度积常数是10-35.4。c点加入20mL硫化钠溶液,硫化钠过量,溶液中硫离子浓度是![]() ,所以根据溶度积常数可知c点溶液中c(Cu2+)=
,所以根据溶度积常数可知c点溶液中c(Cu2+)= 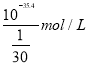 =3×10-34.4mol/L,C正确;D、c点加入20mL硫化钠溶液,由于有CuS沉淀生成,所以根据氯离子和硫原子守恒可知溶液中n(S2-)+n(HS-)+n(H2S)<n(Cl-),D错误;答案选C。
=3×10-34.4mol/L,C正确;D、c点加入20mL硫化钠溶液,由于有CuS沉淀生成,所以根据氯离子和硫原子守恒可知溶液中n(S2-)+n(HS-)+n(H2S)<n(Cl-),D错误;答案选C。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.氯水放置一段时间,pH增大
B.盛有浓硫酸的试剂瓶敞口放置,质量会减轻
C.SO2能使品红溶液褪色
D.硅在自然界主要以单质形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】上世纪80年代后期人们逐渐认识到,NO在人体内起着多方面的重要生理作用。下列关于NO的说法不正确的是
A. NO对臭氧层有破坏作用 B. NO是造成光化学烟雾的因素之一
C. NO是汽车尾气的有害成分之一 D. NO分子所含电子总数为偶数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:SO3的相对分子质量是M,一个氧原子的质量是ag,一个硫原子中有b个中子,则一个硫原子的质子数是(阿伏伽德罗常数用NA表示)( )
A.M﹣3aNA﹣b
B.M﹣3aNA+b
C.[(M÷NA)﹣3a﹣b]
D.[M÷(3a﹣b)NA]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的(V) 的关系如图所示,试回答:

(1)0到a点之间的反应的离子方程式__________
(2)a到b点之间的反应的离子方程式__________
(3)b点之后的反应的离子方程式______________
(4)c 点CO2的体积__________mL(同温同压下)。
(5) 混合溶液中Ba(OH)2和NaOH 的物质的量之比为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个容积均为1L的恒温恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下发生反应3CO(g)+3H2(g)![]() (CH3)2O(g)+CO2(g)(不发生其他反应),CO的平衡转化率与温度和压强的关系加下图所示。
(CH3)2O(g)+CO2(g)(不发生其他反应),CO的平衡转化率与温度和压强的关系加下图所示。
容器 | 起始物质的量/mol | 平衡 转化率 | |||
CO | H2 | (CH3)2O | CO2 | CO | |
Ⅰ | 0.3 | 0.3 | 0 | 0 | 50% |
Ⅱ | 0.3 | 0.3 | 0 | 0.1 | |
Ⅲ | 0 | 0 | 0.2 | 0.4 | |

下列说法正确的是( )
A. 该反应的△H<0,图中压强p1>p2
B. 达到平衡时,容器Ⅱ中CO的平衡转化率大于50%
C. 达到平衡时,容器Ⅰ与容器Ⅱ的总压强之比小于4∶5
D. 达到平衡时,容器Ⅲ中n[(CH3)2O]是容器Ⅱ中的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 纳米材料是指一种称为“纳米”的新物质制成的材料
B. 复合材料有强度高、质量轻、耐高温、耐腐蚀等性能,其综合性质超过单一材料
C. 光导纤维是以二氧化硅为主要原料制成的
D. 合成纤维的主要原料是石油、天然气、煤等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是制造光电池的一种原料,人体缺少硒就会得“克山病”。从电解精炼铜的阳极泥中提取硒的流程如下,已知阳极泥中硒以Se、Ag2Se、Cu2Se等形式存在:

请回答下列问题:
(1)电解精炼铜时,粗铜与电源的_____(填“正极”或“负极”)相连。
(2)SeO2溶于水得到H2SeO3(Ka1=3.5×10-3,Ka2=5.0×10-8),常温下亚硒酸溶液与少量氢氧化钠溶液反应的离子方程式为:_________________,反应所得的盐形成的溶液pH____7,(填>、<或=)原因是________________________________(用相关数据及必要的文字说明)
(3)亚硒酸溶液与SO2反应制硒的化学方程式为_____________________________。电解亚硒酸溶液可制得强酸H2SeO4,则电解时的阴极反应式为________________。
(4)上述硒的提取过程中除了焙烧过程中浓硫酸有强烈的腐蚀性外,还存在的主要问题是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com