
| Ԫ������ | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� |
ԭ�Ӱ뾶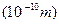 | 1.86 | 1.52 | 0.66 | 1.43 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| ���̬ | +1 | +1 | ���� | +3 | +4 | +5 | +7 | +1 | +5 | ���� |
| ��ͼ�̬ | ���� | ���� | ��2 | ���� | ���� | ��3 | ��1 | ���� | ��3 | ��1 |
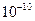 m����Ԫ�������ڱ��е�λ����
m����Ԫ�������ڱ��е�λ���� 
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
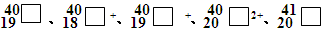 ��������Ԫ�ط���δд����������������Ԫ�ص�������
��������Ԫ�ط���δд����������������Ԫ�ص�������| A��2�� | B��3�� | C��4�� | D��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
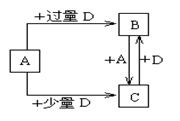
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HClO4 H2SO4 H3PO4 HSiO4 |
| B��HClO4 HClO3 HClO2 HClO |
| C��H2SO4 H2SO3 HNO3 HNO2 |
| D��HClO4H2SO4 H2SO3 H2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڢ�A��Ԫ��藍�Cs������ˮ���ҷ�Ӧ���ų����� |
| B���ڢ�A��Ԫ���裨Tl��������������ˮ����ļ��ԣ�Tl(OH)3�� Al(OH)3 |
| C���ڢ�A��Ԫ������Se�����⻯����ȶ��ԣ�H2Se �� H2O |
| D���ڢ�A��Ԫ������At��Ϊ��ɫ���壬������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2m+8-nROm | B��H2m-8+nROm | C��H2ROm | D��H2mROm |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Xԭ��������������˥���
Xԭ��������������˥���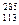 X�������й������У���ȷ����
X�������й������У���ȷ����| A��115��Ԫ��˥���113��Ԫ���ǻ�ѧ�仯 |
B��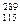 X�� X��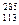 X�����ֺ��� X�����ֺ��� |
C��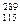 X����������������֮��Ϊ174 X����������������֮��Ϊ174 |
| D��113��Ԫ��λ�����ڱ��ڰ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com