
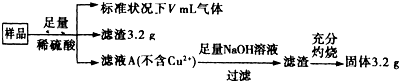
| A、滤液A中的阳离子为Fe3+、Fe2+、H+ |
| B、V=896 |
| C、样品中CuO的质量为4.0g |
| D、样品中Fe元素的质量为2.24g |
| 3.2g |
| 64g/mol |
| 3.2g |
| 160g/mol |
| 5.76g-3.2g-2.24g |
| 16g/mol |


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
| A、H2在负极发生氧化反应 |
| B、燃料电池的化学能可以全部转化为电能 |
| C、产物为无污染的水,属于环境友好电池 |
| D、供电时的总反应为:2H2+O2=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜粉中混有少量的镁粉和铝粉,可加稀盐酸除去 |
| B、用萃取的方法分离汽油和煤油 |
| C、用溶解和过滤的方法分离NaNO3和KCl |
| D、将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2(SO4)3溶液 |
| B、稀硫酸 |
| C、AgNO3溶液 |
| D、CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该物质在一定条件下能发生消去反应、加成反应、取代反应 |
| B、葛根素的分子式为C21H22O9 |
| C、该物质一个分子中含有5个手性碳原子 |
| D、一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸的分子式为CH3COOH,属于弱电解质 |
| B、食醋中含有乙酸,乙酸可由乙醇氧化得到 |
| C、乙醇中是否含有水,可用无水硫酸铜来检验 |
| D、乙醇和乙酸的熔点和沸点都比C2H6、C2H4的熔点和沸点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22g氧气和26g臭氧所含氧原子总数为3 NA | ||
| B、常温常压下,金属和酸反应,若生成2g 氢气,则有2mol电子发生转移 | ||
C、标准状况下,1L H2O约含有
| ||
| D、常温常压下,1mol氮气含有阿伏加德罗常数个氮分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/L | 测得生成沉淀质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 1 |
| 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com