
| A. | 标准状况下,15g二氧化硅含有的分子数为0.25NA | |
| B. | 标准状况下,14g氮气含有的核外电子数为5NA | |
| C. | 标准状况下,22.4L任意比的氢气和氮气的混合气体中含有的分子总数均为2NA | |
| D. | 标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为2NA |
分析 A.二氧化硅是原子晶体,无二氧化硅分子;
B.氮气分子由氮原子构成,根据n=$\frac{m}{M}$计算氮原子的物质的量,再根据N=nNA计算氮原子数;
C.根据n=$\frac{{V}_{\;}}{{V}_{m}}$=$\frac{N}{{N}_{A}}$计算;
D.根据生成氢气的物质的量计算反应中转移的电子数.
解答 解:A.二氧化硅是原子构成的原子晶体,无分子存在,故A错误;
B.14g氮气含有的原子数为$\frac{14g}{14g/mol}$×NAmol-1=NA,每个分子中含电子数7,14g氮气含有的核外电子数为7NA,故B错误;
C.由n=$\frac{{V}_{\;}}{{V}_{m}}$=$\frac{N}{{N}_{A}}$可知,22.4L任意比的氢气和氯气的混合气体的物质的量为1mol,分子数为NA,故C错误;
D.铝与氢氧化钠溶液反应中氢元素化合价由+1价降低为0价,反应生成1mol氢气时,转移的电子数为1mol×2×NAmol-1=2NA,故D正确;
故选D.
点评 本题考查常用化学计量数的有关计算,难度不大,注意气体摩尔体积的使用条件与范围,物质结构和氧化还原反应电子转移的计算应用.


科目:高中化学 来源: 题型:选择题
| A. | 电解质的电离过程就是产生自由移动离子的过程 | |
| B. | 碳酸钙在水中难溶,但被溶解的碳酸钙全部电离,所以碳酸钙是强电解质 | |
| C. | 氯气和氨气的水溶液导电性都很好,所以它们是强电解质 | |
| D. | 水难电离,纯水几乎不导电,所以水是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知,C2H4(g)+H2(g)═C2H6(g)△H=-137.0KJ/mol,乙烯与H2加成时放出68.5KJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA | |
| C. | 100g 17%的H2O2溶液中,极性共价键的数目为NA | |
| D. | 室温下向1L pH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3 | B. | H2C5(线状) | C. | 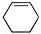 | D. | CH2═CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2O、C2H4O2、C6H12O6 | B. | H2、CO、CH3OH | ||
| C. | CH2═CH2、C2H5OH、HOCH2CH2COOH | D. | C6H6、C5H12、C7H6O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 新制氯水中的所有物质都是电解质 | |
| C. | 氮氧化物、二氧化硫是形成酸雨的主要物质 | |
| D. | 制造光导纤维的原料是晶体硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去硬脂酸钠溶液中的甘油方法是:往溶液中加入饱和食盐水,分液 | |
| B. | 治疗疟疾的青蒿素(如图)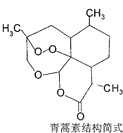 ,分子式是C15H20O5 ,分子式是C15H20O5 | |
| C. | 有机物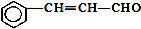 可发生加成反应、氧化反应、还原反应和聚合反应 可发生加成反应、氧化反应、还原反应和聚合反应 | |
| D. | 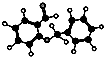 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 右图所示的有机物分子式为C14H12O2,不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用米汤检验食盐中是否含碘酸钾(KIO3) | |
| B. | 用食醋除去暖水瓶中的薄层水垢 | |
| C. | 医用酒精的浓度通常为75%,可用于杀菌消毒 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com