
 ����ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�ⷴӦ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
����ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�ⷴӦ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�| T��K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
���� ��1��ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ����֪��CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ•mol-1��-285.8kJ•mol-1����H2O��1���TH2O��g����H3=44.0kJ•mol-1����֪�Ȼ�ѧ����ʽa��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0kJ•mol-1��b��H2��g��+$\frac{1}{2}$O2��g��=H2O��1����H=-285.8kJ•mol-1��c��H2O��1���TH2O��g����H3=44.0kJ•mol-1�����ø�˹���ɿɼ���CO2��g��+H2��g��?CO��g��+H2O��g���ķ�Ӧ�ȣ�
��2����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H1=-53.7kJ•mol-8 ��֪���CO2ת��ΪCH3OHƽ��ת���ʣ�Ӧʹƽ���������ƶ����ɽ����¶ȣ�����Ũ�ȣ�
��3����ͬ�Ĵ����Ĵ�������ͬ���Ҵ�������ѡ���ԣ�
��4������������ɽ��ͷ�Ӧ�Ļ�ܣ�������Խǿ�����Խ�ͣ�����Ӧ�Ȳ��䣻
��5��CO2Ҳ��������ˮ��Һ��ͨ��������ɼ״���ӦΪ���ص�������Ӧ������ԭ���ɼ״���
��� �⣺��1��ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ���÷�Ӧ��ƽ�ⳣ��Ϊ��K=$\frac{c��C{H}_{3}OH��•c��{H}_{2}O��}{c��C{O}_{2}��•{c}^{3}��{H}_{2}��}$��
��֪��CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ•mol-1��-285.8kJ•mol-1����H2O��1���TH2O��g����H3=44.0kJ•mol-1����֪�Ȼ�ѧ����ʽa��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0kJ•mol-1��b��H2��g��+$\frac{1}{2}$O2��g��=H2O��1����H=-285.8kJ•mol-1��c��H2O��1���TH2O��g����H3=44.0kJ•mol-1��
�ɸ�˹���ɽ�b-a+c�ɵã�CO2��g��+H2��g��?CO��g��+H2O��g����H2 =��-285.8+283.0+44��kJ•mol-1=+41.2kJ•mol-1��
�ʴ�Ϊ��$\frac{c��C{H}_{3}OH��•c��{H}_{2}O��}{c��C{O}_{2}��•{c}^{3}��{H}_{2}��}$��+41.2��
��2��A��ʹ�ô���Cat.1��ƽ�ⲻ�ƶ����������ת���ʣ���A����
B��ʹ�ô���Cat.2���������ת���ʣ���B����
C�����ͷ�Ӧ�¶ȣ�ƽ�������ƶ���������ת���ʣ���C��ȷ��
D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ�ȣ��������ƶ���������ת���ʣ���D��ȷ��
E������ CO2��H2�ij�ʼͶ�ϱȣ�������������ת���ʣ�������̼��ת���ʼ�С����E����
�ʴ�Ϊ��CD��
��3���ӱ������ݷ���������ͬ�¶��£���ͬ�Ĵ���������̼��ת���ʲ�ͬ��˵����ͬ�Ĵ����Ĵ�������ͬ����ͬ�Ĵ�����ͬ���¶ȣ�������̼��ת���ʲ�ͬ�����¶ȸߵ�ת���ʴ���Ϊ����ӦΪ���ȷ�Ӧ��˵������������δ�ﵽƽ�����ݣ�
�ʴ�Ϊ���������ݱ�����ʱδ�ﵽƽ�⣬��ͬ�Ĵ����Է�Ӧ��Ĵ�������ͬ������ڸ�ʱ���¶Լ״�ѡ������Ӱ�죻
��4���ӱ������ݷ������ڴ���Cat.2�������£��״���ѡ���Ը���˵������Cat.2�Է�Ӧ���Ч�����ã������ܽ��ͷ�Ӧ�Ļ�ܣ�˵��ʹ�ô���Cat.2�ķ�Ӧ�����л�ܸ��ͣ���ͼΪ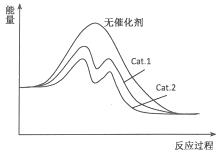 ��
��
�ʴ�Ϊ�� ��
��
��5��CO2Ҳ��������ˮ��Һ��ͨ��������ɼ״���CԪ�ػ��ϼ۽��ͣ�����ԭ��ӦΪ���ص�������Ӧ���缫����ʽΪ��CO2+6H++6e-=CH3OH+H2O��
�ʴ�Ϊ������CO2+6H++6e-=CH3OH+H2O��
���� ���⿼���Ϊ�ۺϣ��漰��ѧƽ��ļ��㣬ƽ���ƶ��Լ��Ȼ�ѧ����ʽ���绯ѧ��֪ʶ��Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ�������ѧ���ķ������������������Ŀ��飬ע����ո�˹���ɵ�Ӧ�ã����صĹ���ԭ����֪ʶ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��Ӧ�ﵽƽ��������������䣬ֻ�ı�ѹǿ��ƽ�ⲻ�ƶ� | |
| B�� | ������Ӧ�����е�ƽ����Է����������� | |
| C�� | ��λʱ���ڷ�Ӧ��Ũ�ȵļ��ٵ���������Ũ�ȵ����� | |
| D�� | ����ǰ10s��B������xmol������ǰ20s��A����С��2xmol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �÷�Ӧ�ġ�H��0 | B�� | ��ƽ��ʱ��3v��H2����=v��CO2���� | ||
| C�� | a���Ӧ��H2��ƽ��ת����Ϊ90% | D�� | b���Ӧ��ƽ�ⳣ��Kֵ����c�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ���� | �� | �� | �� | �� |
| A | 2mol | 1mol | 2mol | 1mol |
| B | 1mol | 1mol | 2mol | 2mol |
| A�� | A��ת���ʣ����������ң��� | B�� | A��ת���ʣ������ң������� | ||
| C�� | B��ת���ʣ������ף��ң��� | D�� | B��ת���ʣ��ף��ң������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | 0 | 50 | 150 | 250 | 350 |
| n��NH3�� | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �¶ȣ���C�� | ��ʼŨ�ȣ�mol•L-1�� | ƽ��Ũ�ȣ�mol•L-1�� | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | ||
| �� | T | 1 | 3 | 0 | 0.2 | 1.4 | 0.8 |
| �� | T | 1.5 | 4.6 | 0.1 | b1 | b2 | b3 |
| �� | T+30 | 1 | 3 | 0 | 0.25 | 1.5 | 0.75 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
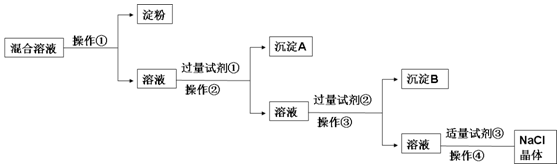
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش�
�������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com