
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是 ( )
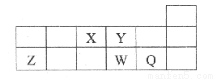
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rx> rY> rz> rQ
C,离子Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:实验题
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是 。
(2)将a中的溶液加热至100 ℃,从b中缓缓滴加40 g苯乙腈( )到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称是 ,反应结束后加适量冷水,再分离出苯乙酸(
)到硫酸溶液中,然后升温至130 ℃继续反应。仪器c的名称是 ,反应结束后加适量冷水,再分离出苯乙酸( )粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
)粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A 分液漏斗B 漏斗C 烧杯D.直形冷凝管E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸()的产率是 。
(4)用CuCl2? 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
若阿伏加德罗常数的数值用NA表示,下列说法正确的是( )
A.标准状况下,1.12L氦气所含原子数为0.1NA B.1.6gNH2-离子所含质子数为NA
C.22.4 LHCl溶于水,溶液中H+数为NA D.9g D2O所含的中子数为4.5NA
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市高三六校第二次联考理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】(15分)
氮化钛( Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金代替品。以TiCl4为原料,经过一系列反应(如图所示),可以制得Ti3N4和纳米TiO2请回答下列问题:
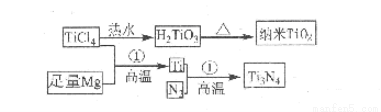
(1)反应①为置换反应,写出该反应的化学方程式 ;TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为 。
(2)元素周期表中Ti元素位于第 周期 族。与Ti相邻的元素Zr的基态原子外围电子排布式为 ,
(3)纳米TiO2是一种应用广泛的催化剂,纳米Ti02催化的一个实验如图所示。
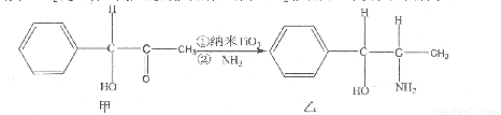
化合物甲的分子中采取sp2方式杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。
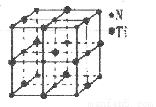
(4)有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有 个N原子,晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为 g.cm-3(NA为阿伏加德常数的数值,只列算式)。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市高三六校第二次联考理综化学试卷(解析版) 题型:选择题
分子式为C3H2Cl6的同分异构体共有(不考虑立体异构)( )
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市第二学期期末教学质量测试高二化学试卷(解析版) 题型:实验题
某小组通过实验研究Na2O2与水的反应?

(1)Na2O2与水反应的化学方程式是 ?
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应?
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂 (填化学式),有气体产生?
Ⅱ.乙同学查阅资料获悉:用KMnO4(被还原为 )可以测定H2O2的含量?
)可以测定H2O2的含量?
取3mL溶液a稀释至15mL,用稀H2SO4酸化,再逐滴加入0.0045 KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗10mL KMnO4溶液?
KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗10mL KMnO4溶液?
①KMnO4与H2O2反应的离子方程式是 ?
②溶液a中 ?
?
③溶液褪色速率开始较慢后变快的原因可能是 ?
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅰ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1 NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色,该过程无明显热效应?
NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色,该过程无明显热效应?
Ⅱ.向0.1 NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化?从实验Ⅰ和Ⅱ中,可得出的结论是 ?
NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化?从实验Ⅰ和Ⅱ中,可得出的结论是 ?
查看答案和解析>>
科目:高中化学 来源:2013-2014江西八一中学、洪都中学下学期期中考试高一化学试卷(解析版) 题型:填空题
(12分) 类推法是科学学习的重要方法之一
⑴ 下列类推结论正确的是
| 类比对象 | 结论 |
A | Cl2+H2O | I2+H2O |
B | C+2CuO === 2Cu+CO2↑(条件:加热) | C+SiO2 === Si+ CO2↑(条件:加热) |
C | Na2O+H2O == 2NaOH | CuO+H2O == Cu(OH)2 |
D | Ca(ClO)2+CO2+H2O== CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O== CaSO3↓+2HClO |
⑵ 在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质,请结合元素周期律完成下列问题:
元素 | 8O | 16S | 34Se | 52Te |
单质熔点(℃) | -218.4 | 113 |
| 450 |
单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 |
|
原子半径 | 逐渐增大 | |||
单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
硒的熔点范围可能是_______ ;
② 碲的化合价可能的范围_______ ;
③ 硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是 (填化学式);
④ 氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:选择题
化学与社会、生产、生活密切相关。下列说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.“地沟油”禁止食用,但可以用来制肥皂
C.煤经过气化和液化等物理变化可转化为清洁燃料
D.纤维素、油脂、蛋白质均是天然高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com